
分析 根据物质的性质、化学方程式的书写方法、温度的控制、以及流程的优点进行分析解答即可.
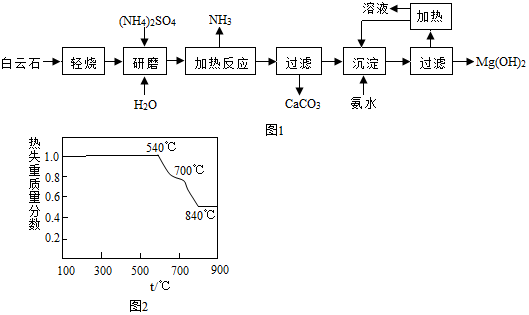
解答 解:(1)白云石属于混合物,碳酸镁分解生成氧化镁和二氧化碳,根据图2可以看出温度不能超过700℃,故填:混合,MgCO3$\frac{\underline{\;\;△\;\;}}{\;}$MgO+CO2↑,700℃;
(2)硫酸铵与氧化镁在加热条件下反应生成硫酸镁、氨气和水,故填:(NH4)2SO4+MgO$\frac{\underline{\;\;△\;\;}}{\;}$MgSO4+2 NH3↑+H2O;
(3)根据流程图可以看出,氨气和硫酸铵能循环利用,故填:NH3;
(4)采用轻烧白云石的方法制备氢氧化镁,能减少能源消耗、便于CaCO3分离,故填:减少能源消耗,便于CaCO3分离.
点评 本题考查的是常见的物质的制备的知识,完成此题,可以依据物质的性质结合流程图进行.


科目:初中化学 来源: 题型:选择题
| A. | 火场逃生时在有烟雾的地方应匍匐前进 | |
| B. | 为了防止水污染,农业上要合理使用化肥、农药 | |
| C. | 回收废旧电池,即可节约金属资源又可减少环境污染 | |
| D. | 人体缺锌会引起生长发育缓慢,因此锌元素的摄入量越多越好 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
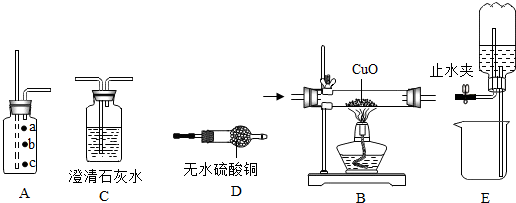
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 过滤、煮沸、蒸馏操作中煮沸的净水程度最高 | |
| B. | 水体有自净能力,未经处理的生活污水可随意排放 | |
| C. | 空气中含量最多的单质是氧气 | |
| D. | 空气中的二氧化碳是植物进行光合作用必需的物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com