
分析 铜不能和稀盐酸反应,锌和稀盐酸反应生成氯化锌和氢气,反应前后的质量差即为反应生成氢气的质量,根据氢气的质量可以计算锌的质量,进一步可以计算该黄铜中铜的质量分数.
解答 解:(1)反应生成氢气的质量为:20g+50g-69.8g=0.2g,
答:生成了0.2g氢气.
(2)设锌的质量为x,
Zn+2HCl═ZnCl2+H2↑,
65 2
x 0.2g
$\frac{65}{x}$=$\frac{2}{0.2g}$,
x=6.5g,
该黄铜中铜的质量分数为:$\frac{20g-6.5g}{20g}$×100%=67.5%,
答:该黄铜中铜的质量分数为67.5%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 2P+5O2═P2O5 | B. | CO+O2$\frac{\underline{\;点燃\;}}{\;}$ CO2 | ||
| C. | 3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$ Fe3O4 | D. | H2O2═H2O+O2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
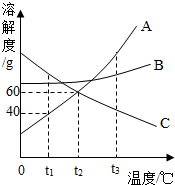 如图是 A、B、C三种物质的溶解度曲线.请回答:
如图是 A、B、C三种物质的溶解度曲线.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
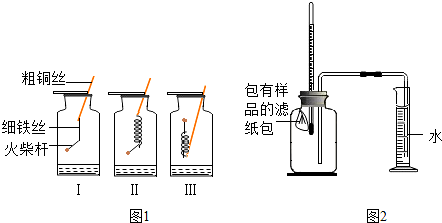
| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| 1 | 1g铁粉、0.2g碳、10滴水 | 100 | 72 | 约120 |
| 2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 72 | 约70 |
| 3 | / | / | / |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
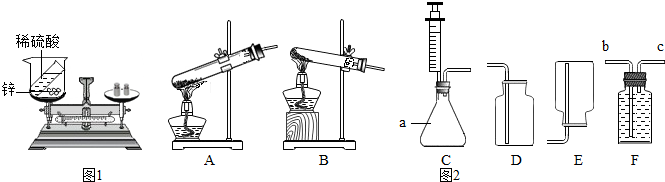
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com