
| A. | Na2CO3 HCl H2SO4 NaNO3 | B. | K2CO3 H2SO4 HNO3 BaCl2 | ||
| C. | HCl AgNO3 HNO3 NaCl | D. | NaOH FeCl3 MgCl2 BaCl2 |
分析 在不另加试剂就能鉴别的题目中,首先观察有无有特殊颜色的物质,若有,将有颜色的溶液鉴别出来,然后再借用这种溶液鉴别其它溶液把其它没有确定出的物质确定出来;若都没有颜色就将溶液两两混合,根据混合后的现象进行分析鉴别.
解答 解:A、组内四种物质的溶液两两混合时,Na2CO3溶液与HCl、H2SO4溶液反应均能产生无色气体,但其余两两混合均没有明显现象,故不加其他试剂无法鉴别.
B、组内四种物质的溶液两两混合时,其中有一种溶液与其它三种溶液混合时出现一次白色沉淀和两次放出气体,该溶液为K2CO3溶液;与K2CO3溶液产生气体的溶液为H2SO4、HNO3,产生白色沉淀的为BaCl2;再将氯化钡溶液分别滴加至硫酸、硝酸中,与BaCl2溶液混合产生白色沉淀的是硫酸,无明显变化的是硝酸;故不加其他试剂可以鉴别.
C、组内四种物质的溶液两两混合时,AgNO3溶液与HCl、NaCl溶液反应均能产生白色沉淀,但其余两两混合均没有明显现象,故不加其他试剂无法鉴别.
D、FeCl3溶液是黄色的,能与FeCl3溶液反应产生红褐色沉淀的是的是NaOH溶液,能与NaOH溶液反应产生白色沉淀的是MgCl2溶液,无明显变化的是氯化钡溶液,故不加其他试剂可以鉴别.
故选:BD.
点评 解答不另加试剂就能鉴别的题目时,若选项中有带色的离子,首先鉴别,然后再鉴别其它的物质;若都没有颜色,可将溶液两两混合,根据混合后的现象进行鉴别.


 目标测试系列答案
目标测试系列答案科目:初中化学 来源: 题型:解答题
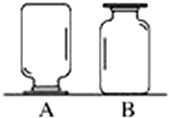 如图,在实验台上放置两瓶气体,集气瓶A、B中盛有二氧化碳(密度比空气的大)、氧气(密度比空气的大)、氢气(密度比空气的小)中的一种.小刚和小强想对瓶中气体进行探究:
如图,在实验台上放置两瓶气体,集气瓶A、B中盛有二氧化碳(密度比空气的大)、氧气(密度比空气的大)、氢气(密度比空气的小)中的一种.小刚和小强想对瓶中气体进行探究:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
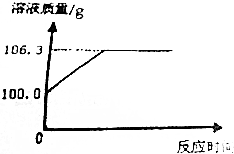 将10.0g铜锌合金的粉末置于烧杯中,然后向其中加入100.0g的稀硫酸溶液,恰好完全反应,测得烧杯中溶液质量的变化关系如下图所示(不考虑物质耗损).
将10.0g铜锌合金的粉末置于烧杯中,然后向其中加入100.0g的稀硫酸溶液,恰好完全反应,测得烧杯中溶液质量的变化关系如下图所示(不考虑物质耗损).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
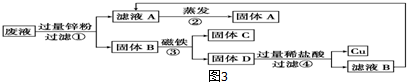
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com