
分析 固体混合物中碳酸钠与盐酸反应放出气体二氧化碳,根据质量守恒定律计算出二氧化碳的质量,然后利用化学方程式计算混合固体中碳酸钠的质量和生成的氯化钠的质量,所得溶液中溶质的质量即可计算解决.
解答 解:(1)反应生成二氧化碳的质量=12g+98.6g-106.2g=4.4g;故填:4.4g;
(2)设碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{4.4g}$
x=10.6g
y=11.7g
所得氯化钠溶液中溶质的质量=11.7g+(12g-10.6g)=13.1g
答:最终得到的氯化钠溶液中,溶质的质量13.1g.
点评 根据质量守恒定律,反应后所得溶液的质量=固体混合物的质量+稀盐酸的质量-生成二氧化碳气体的质量,是解题的关键所在.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:初中化学 来源: 题型:解答题
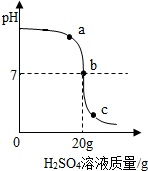 化学小组探究酸碱中和反应时,利用溶质质量分数为4.9%的稀硫酸来测定10gNaOH溶液样品的溶质质量分数,用数字化传感器测得溶液中pH的变化如图所示
化学小组探究酸碱中和反应时,利用溶质质量分数为4.9%的稀硫酸来测定10gNaOH溶液样品的溶质质量分数,用数字化传感器测得溶液中pH的变化如图所示查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 氮氧化物(NOx)等气体破坏人类生存的环境.
氮氧化物(NOx)等气体破坏人类生存的环境.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
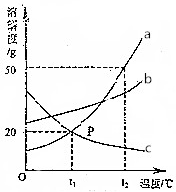 a、b、c三种物质的溶解度曲线如图所示.下列叙述正确的是( )
a、b、c三种物质的溶解度曲线如图所示.下列叙述正确的是( )| A. | t1℃时,a、c的饱和溶液的溶质质量一定相等 | |
| B. | t2℃时,a、b各50g分别放入100g水中均能全部溶解 | |
| C. | 将a的溶液从t2℃降至t1℃时,其溶质质量分数不一定减小 | |
| D. | 将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液中溶质质量分数最大的是a. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com