

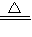 NH3↑+CO2↑+H2O;氨气的水溶液显碱性,能使酚酞试液变成红色,虽然二氧化碳的水溶液显酸性,应该不能使酚酞试液变色,但根据最终的现象是酚酞试液变成了红色,说明溶液最终表现为碱性,是由于氨气在水中的溶解性大于二氧化碳的缘故;
NH3↑+CO2↑+H2O;氨气的水溶液显碱性,能使酚酞试液变成红色,虽然二氧化碳的水溶液显酸性,应该不能使酚酞试液变色,但根据最终的现象是酚酞试液变成了红色,说明溶液最终表现为碱性,是由于氨气在水中的溶解性大于二氧化碳的缘故;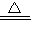 NH3↑+CO2↑+H2O;大于;(4)用热水浇注温度上升的快,微粒的碰撞几率大;【设计方案】(1)有气泡产生,溶液由无色变为蓝色;试管底部有绿色粉末状固体;上升;Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑.
NH3↑+CO2↑+H2O;大于;(4)用热水浇注温度上升的快,微粒的碰撞几率大;【设计方案】(1)有气泡产生,溶液由无色变为蓝色;试管底部有绿色粉末状固体;上升;Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑.

科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省苏州市初三中考二模化学试卷(解析版) 题型:填空题
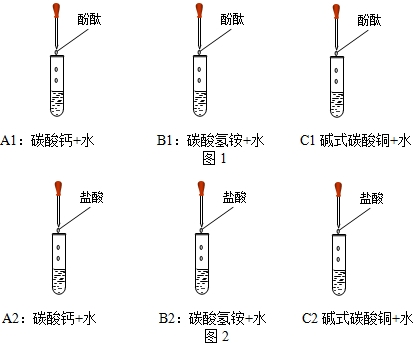
(8分)对碳酸钙、碳酸氢铵、碱式碳酸铜三种碳酸盐的性质比较:
在1、2、3三试管中依次加入碳酸钙、碳酸氢铵、碱式碳酸铜各少量固体(各2份)。
第一份:在1、2、3三试管中各倒入少些水并振荡至充分溶解,用玻璃棒蘸取液体并与标准比色卡对照,可测定三种物质的pH 。实验时要多次使用玻璃棒,所以,每次测定后应对玻璃棒进行 处理。根据你的实验结果,可以得出上述三种碳酸盐水溶液的pH由大到小的顺序是(填试管编号):
试管 >试管 >试管 。(1分)
将1、2、3三试管置于烧杯内热水水浴。根据你的实验结果和学过的知识,可以得出
三种碳酸盐的热稳定性由强至弱的顺序是(填化学式):
> > 。(1分)
按盐的组成分类,碳酸钙、碳酸氢铵、碱式碳酸铜依次为正盐、酸式盐和碱式盐。初步推想,正盐、酸式盐和碱式盐的热稳定性由强至弱的顺序应该是:
> > 。(1分)
第二份:在1、2、3三试管中分别加入稀盐酸,都能观察到 。
要鉴定该气体,你的操作方法是: 。
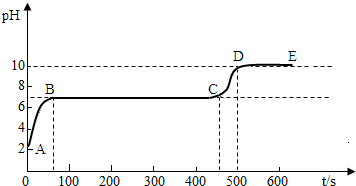
碳酸钙和适量稀盐酸反应至气泡逸出不明显后,测得其残留液pH等于2。 此时取适量
反应后溶液,逐滴滴入碳酸钠溶液,并用pH数字探测仪连续监测,得曲线如下[ pH为纵坐标,时间s(秒)为横坐标]:
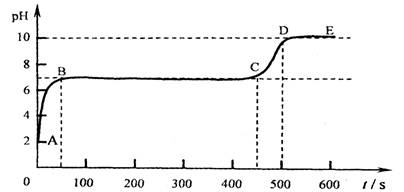
①写出BC“平台”段化学方程式 ;
②CD段上升的原因是: 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com