
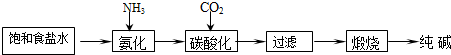
| 实验步骤 | 实验现象 | 实验结论 |
如图装置,把少量样品放入a试管中加热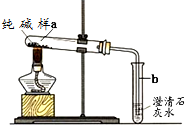 | b试管澄清石灰水 没变浑浊 | 纯碱样品中没有NaHCO3 |
| 取样品少量,溶解,加足量稀硝酸,再滴加硝酸银溶液 | 有白色沉淀产生 | 纯碱样品中有NaCl |
分析 【实验设计】根据碳酸钠和碳酸氢钠的化学性质以及氯离子的检验方法来分析;
【研究课题2】【实验方案Ⅰ】为了测定碳酸钠的含量,加入的氯化钙必须是足量的;根据操作的方便性来分析;
【数据处理】根据化学方程式进行解答.
【分析与讨论】(1)使生成的CO2全部被NaOH溶液吸收;
(2)碳酸氢钠与盐酸反应又会生成二氧化碳气体;
【分析与评价】在多次过滤洗涤过程中,物质可能有损失;
【拓展与延伸】根据D装置中发生的两个化学反应结合化学方程式进行计算.
解答 解:【实验设计】因为碳酸氢钠在加热的条件下会分解产生二氧化碳,澄清的石灰水会变浑浊,此时石灰水没有变浑浊,说明固体中不含碳酸氢钠;如果样品中含有氯化钠就能与硝酸银溶液反应生成白色沉淀;
故填:没有;有白色沉淀产生;
【研究课题2】【实验方案Ⅰ】为了测定样品中碳酸钠的质量分数就必须将碳酸钠全部转化为碳酸钙沉淀,故加入的氯化钙溶液必须是足量的;分析操作的方便性,b操作方法是正确的;故填:足量;b;
【数据处理】设其中碳酸钠的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 8g
$\frac{106}{x}$=$\frac{100}{8g}$
x≈8.5g
纯碱样品中碳酸钠的质量分数为:$\frac{8.5g}{10g}$×100%=85%
故填:85%.
【分析与讨论】(1)结束时让空气流通使生成的CO2全部被NaOH溶液吸收;故填:使生成的CO2全部被NaOH溶液吸收;
(2)氯化氢气体与碳酸氢钠溶液反应生成了二氧化碳,导致测量结果偏大,因此不能;故填:否;氯化氢气体与碳酸氢钠溶液反应生成了二氧化碳,导致测量结果偏大;
【分析与评价】在多次洗涤过程中,可能造成沉淀物的损失,故填:多次洗涤造成沉淀物的损失.
点评 本题考查较为综合,侧重于学生的分析能力、计算能力和实验能力的考查,注意把握物质的性质以及反应的实验原理,难度中等.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 其相对分子质量的计算式为12×14×1×12×16×3 | |
| B. | 分子中碳、氢、氧三种元素的原子个数比为14:12:3 | |
| C. | 物质中碳、氢、氧三种元素的质量比为14:1:8 | |
| D. | 其相对分子质量为200 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
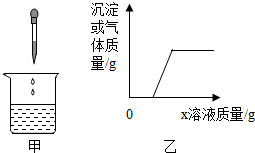 向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入x溶液的质量关系符合图乙的是( )
向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入x溶液的质量关系符合图乙的是( )| 烧杯中的物质 | x溶液 | |
| A | 稀盐酸和硫酸铜溶液 | 烧碱溶液 |
| B | 稀硫酸和稀盐酸 | 氯化钡溶液 |
| C | 镁铝合金 | 稀硫酸 |
| D | 氯化钠和碳酸氢钠溶液 | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 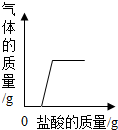 在部分变质的NaOH溶液中滴加稀盐酸 | |
| B. | 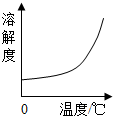 O2的溶解度受温度影响的变化曲线 | |
| C. |  等质量的Mg粉和Fe粉与足量同浓度的稀盐酸反应 | |
| D. | 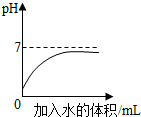 硫酸溶液稀释过程中pH的变化曲线 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
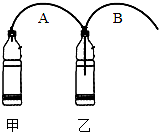 如图所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱.药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过B管从乙瓶导出,即可供人吸氧.
如图所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱.药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过B管从乙瓶导出,即可供人吸氧.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com