
| A. | 原子是构成物质的一种粒子 | B. | 原子质量小、体积小、不断运动 | ||
| C. | 原子是化学变化中的最小粒子 | D. | 原子是由原子核和核外电子构成的 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
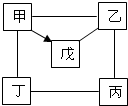 如图示中的“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下可以实现转化.下列四组选项中,符合图示要求的是( )
如图示中的“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下可以实现转化.下列四组选项中,符合图示要求的是( )| 甲 | 乙 | 丙 | 丁 | 戊 | |
| A | Fe | H2SO4 | NaOH | CuCl2 | Fe2O3 |
| B | H2 | CuO | HCl | O2 | CO |
| C | H2SO4 | Fe2O3 | HCl | Zn | CuCl2 |
| D | Na2CO3 | Ca(OH)2 | NaOH | HCl | CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
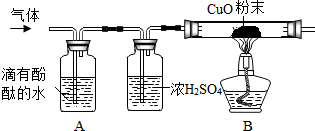
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 蜡烛刚刚熄灭时产生的白烟是二氧化碳气体 | |
| B. | 氢氧化钠固体易潮解,可做某些气体的干燥剂 | |
| C. | 二氧化碳不供给呼吸,不宜作为植物的养料 | |
| D. | 大量使用化石燃料会造成大气污染,应该停止对化石燃料的开采和利用 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 合金:生铁、不锈钢、青铜 | |
| B. | 碱:纯碱、烧碱、氨水 | |
| C. | 盐:高锰酸钾、氯化钠、碳酸氢钠 | |
| D. | 合成材料:塑料、合成纤维、合成橡胶 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe、Ag、CuSO4溶液 | B. | Cu、Ag、FeSO4溶液 | ||
| C. | Fe、Cu、H2SO4溶液 | D. | Ag、FeSO4溶液、CuSO4溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
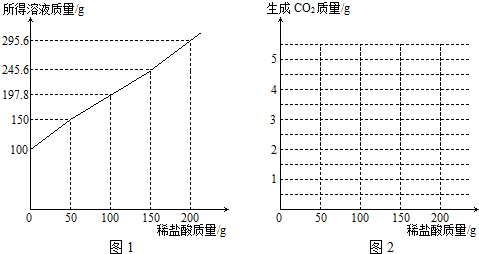
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
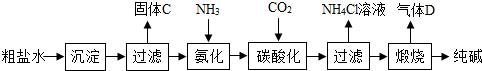
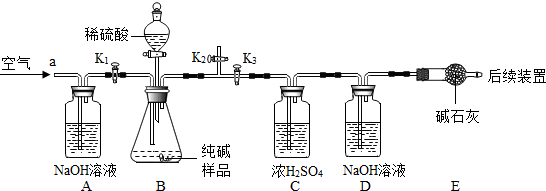
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 乙醇属于可再生能源 | |
| B. | “可燃冰”将成为未来的新能源 | |
| C. | 将煤碳加工成蜂窝煤,能使煤燃烧更充分 | |
| D. | 化学电池是将化学能传化为热能的一种方式 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com