
| A. | Ag+ | B. | Al3+、Ag+、Zn2+ | C. | Al3+、Zn2+ | D. | Ag+、Zn2+ |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学为人类生活提供了许多便利.
化学为人类生活提供了许多便利.| 成分 | 水 | 蛋白质 | 油脂 | 糖类 | 钙 | 磷 | 铁 | 维生素B1 | 维生素B2 |
| 质量分数/% | 89.3 | 4.7 | 1.3 | 2.8 | 0.24 | 0.064 | 1.4 | 0.00006 | 0.00003 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
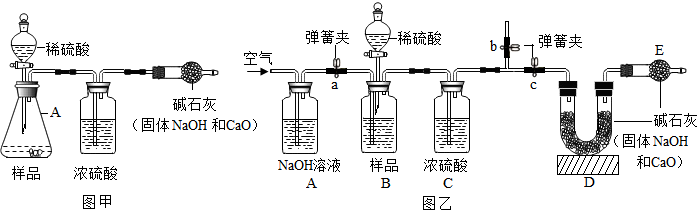

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ③④ | D. | ④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 现象 | 结论 |
| 1取少量蒸馏水滴加紫色石蕊试液. | 溶液不变色. | H2O不能(填“能”或“不能”)使紫色石蕊试液变红色. |
| 2另取少量氯化钠溶液于试管中,向其中滴加紫色石蕊试液. | 溶液不变色 | Cl-不能使紫色石蕊试液变红色. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验序号 | ① | ② | ③ | ④ |
| 水的质量(g) | 10 | 10 | 10 | 10 |
| 加入NaCl的质量(g) | 2 | 3 | 4 | 5 |
| 所得溶液的质量(g) | 12 | 13 | 13.6 | 13.6 |
| A. | ①所得溶液溶质质量分数为20% | |
| B. | ②所得溶液为饱和溶液 | |
| C. | 氯化钠属于可溶性固体 | |
| D. | 所得溶液的溶质质量分数大小关系为:④=③>②>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com