
阳光牌小包装“脱氧剂”成分为Fe粉、活性炭及少量NaCl、水.使用一段时间后,其中的Fe粉会转变成Fe2O3而变质.某化学兴趣小组欲探究使用过的阳光牌“脱氧剂”的变质程度(已变质的Fe粉占变质前Fe粉的质量分数),设计并进行如下探究过程.
步骤(1)取食品包装袋中的阳光牌“脱氧剂”一袋,将里面的固体溶于水,过滤、洗涤、干燥滤渣.
步骤(2)取步骤(1)中的滤渣8.0 g,加入足量的稀H2SO4与滤渣充分反应,过滤、洗涤、干燥得固体1.2 g.
步骤(3)取步骤(2)中的滤液,加入足量的NaOH溶液,得到的固体经洗涤后转移到坩埚中,充分加热、冷却、称量,得到8.0 g Fe2O3(注:滤液中的Fe元素已全部转化为Fe2O3).
求:(1)8.0 g滤渣中Fe和Fe2O3两种物质的总质量.
(2)该“脱氧剂”在未变质时,Fe粉和活性炭的质量之比.
(3)该“脱氧剂”的变质程度.
科目:初中化学 来源: 题型:
| 实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
| ①取食品包装袋中的“脱氧剂”一袋,将里面的固体溶于水,过滤、洗涤、干燥滤渣. | 无 | 无 |
| ②取步骤①中的滤渣8.0 g,加入足量② |
若没有气泡产生. | 证明固体① |
| 若③ |
证明固体肯定含有④ | |
| ③取步骤②中的滤液,加入足量的NaOH溶液,得到的固体经洗涤后转移到坩埚中,充分加热、冷却、称量,得到8.0 g Fe2O3(注:滤液中的Fe元素已全部转化为Fe2O3) | 无 | 确认固体含有⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:广东省模拟题 题型:实验题
查看答案和解析>>
科目:初中化学 来源:2009-2010学年江苏省南京市金陵中学河西分校九年级(下)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目:初中化学 来源:2009-2010学年九年级(下)第一次段考化学试卷(解析版) 题型:解答题
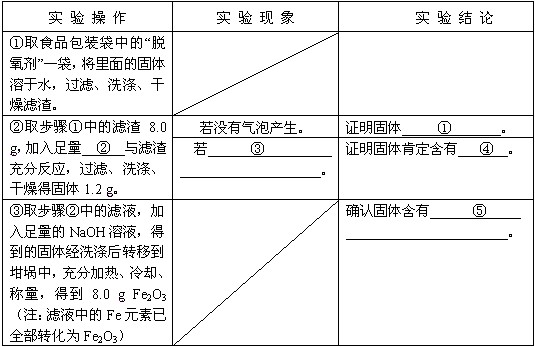
| 实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
| ①取食品包装袋中的“脱氧剂”一袋,将里面的固体溶于水,过滤、洗涤、干燥滤渣. | 无 | 无 |
| ②取步骤①中的滤渣8.0 g,加入足量②______与滤渣充分反应,过滤、洗涤、干燥得固体1.2 g. | 若没有气泡产生. | 证明固体①______. |
| 若③______. | 证明固体肯定含有④______. | |
| ③取步骤②中的滤液,加入足量的NaOH溶液,得到的固体经洗涤后转移到坩埚中,充分加热、冷却、称量,得到8.0 g Fe2O3(注:滤液中的Fe元素已全部转化为Fe2O3) | 无 | 确认固体含有⑤______. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com