
| ||


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:初中化学 来源: 题型:
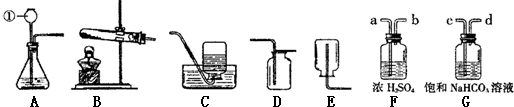
| A、①②③④⑤ |
| B、②①④③⑤ |
| C、②③④①⑤ |
| D、①④②③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:
A、4Fe+3O2
| ||||
B、2KClO3
| ||||
C、4P+5O2
| ||||
D、2C2H2+5O2
|
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
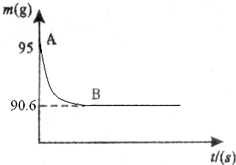 鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中碳酸钙的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除碳酸钙外的其他成分不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所有盐酸刚好消耗了加入量的一半.试计算:
鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中碳酸钙的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除碳酸钙外的其他成分不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所有盐酸刚好消耗了加入量的一半.试计算:查看答案和解析>>
科目:初中化学 来源: 题型:
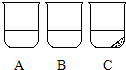 如图,在A、B、C三只烧杯中盛有等质量的水,然后依次加入30g、40g、50g蔗糖,用玻璃棒充分搅拌溶解,最后情况如图:请你判断
如图,在A、B、C三只烧杯中盛有等质量的水,然后依次加入30g、40g、50g蔗糖,用玻璃棒充分搅拌溶解,最后情况如图:请你判断查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com