
| A.NaCl、H2O | B.NaOH、CuSO4 | C.Cu、AgNO3 | D.CO2、Ca(OH)2 |
科目:初中化学 来源: 题型:阅读理解
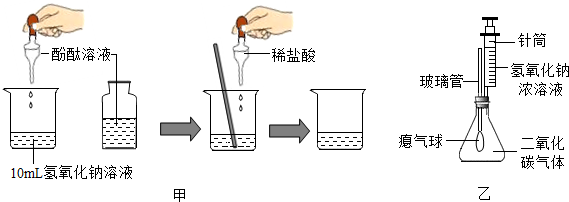
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上 层清液于试管中, 加入过量氯化钙 溶液,静置. |
①没有白色沉淀,溶液呈红色. | |
| ②有白色沉淀,溶液由红色变 为无色 |
||
| ③ |
你的猜想正确. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源: 题型:
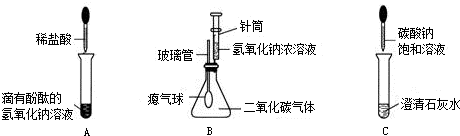
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. | ①有白色沉淀,溶液呈红色. | |
| ② |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
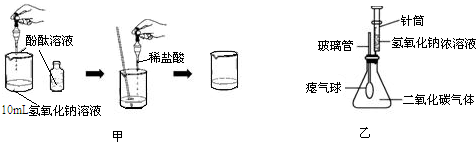
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上 层清液于试管中, 加入过量氯化钙 溶液,静置. | ①没有白色沉淀,溶液呈红色. | ______的猜想正确. |
| ②有白色沉淀,溶液由红色变 为无色 | ______的猜想正确. | |
| ③______ | 你的猜想正确. |
查看答案和解析>>
科目:初中化学 来源:2012年湖北省仙桃市、天门市、潜江市、江汉油田中考化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com