
下列现象或事实,可用金属活动性作出解释的是()
①黄铜(铜锌合金)外观与黄金相似,但可将两者放入稀盐酸中加以区别
②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强
③用硫酸铜、石灰水配置农药波尔多液时,不能用铁制容器.
A. ② B. ①③ C. ②③ D. ①②③
科目:初中化学 来源: 题型:
某金属冶炼厂的工业废渣中含有泥沙和某些单质,其中单质含有铜、锌和少部分硫。现欲回收铜和锌,并对硫进行
处理,主要流程如下图所示:
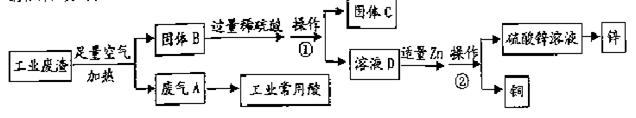 (1)在废气A中,一定含有的有害气体是 (填化学式)。操作①的操作名称是 。
(1)在废气A中,一定含有的有害气体是 (填化学式)。操作①的操作名称是 。
(2)溶液D中含有的溶质是 (填化学式)。
(3)写出加入Zn后发生的化学方程式(写出其中之一即可) 。
查看答案和解析>>
科目:初中化学 来源: 题型:
某实验小组在探究金属的化学性质的时,得到金属与酸反应制取氢气的质量关系(见右下图)。请根据图像信息判断,下列说法正确的是()
A.四种金属与酸反应的速率:Al > Mg > Fe > Zn
B.四种金属的活动性顺序:Mg > Al > Zn > Fe
C.同质量的四种金属与足量酸反应得到氢气的质量:Al > Mg > Fe > Zn
D.Al 、Mg 、Fe、 Zn四种金属与酸反应得到氢气的质量比: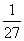 :
: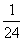 :
: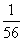 :
:
查看答案和解析>>
科目:初中化学 来源: 题型:
老师在课堂上做钠的性质实验,先用小刀切下绿豆大小的一块,可以看到银白色的金属光泽,再放入滴加过酚酞试液的水中,观察到钠浮在水面上,熔化成闪亮的小球,四处游动,发出“嘶嘶”的响声,溶液变红。反应后产生一种气体,经检验其密度最小且具有可燃性。
根据以上描述,回答下列问题:
⑴钠的物理性质 (答出一条即可)。
⑵解释任一处划线现象的原因 。
⑶如果在实验室中制取该反应产生的气体,收集方法为 。
⑷反应完毕,向溶液中滴加稀盐酸至过量,可观察到的现象为 。
⑸反应完毕,向溶液中通入二氧化碳,无明显现象。现提供固体氢氧化钠、二氧化碳、乙醇和必需的仪器,并查得如下资料。
请设计一个“看得见”的氢氧化钠与二氧化碳反应的实验 。
查看答案和解析>>
科目:初中化学 来源: 题型:
若金属锰在金属活动性顺序中位于铝和锌之间,则下列反应不能发生的是()【提示:MnSO4溶于水】
|
| A. | Mn+2HCl=MnCl2+H2↑ | B. | Fe+MnSO4=FeSO4+Mn |
|
| C. | 2Al+3MnSO4=Al2(SO4)3+3Mn | D. | Mg+MnSO4=MgSO4+Mn |
查看答案和解析>>
科目:初中化学 来源: 题型:
今年5月,吴王夫差剑重返苏州。吴王夫差剑为春秋末期制造的青铜剑,时隔2500年,虽表面有一层蓝色薄锈,但仍寒光逼人,刃锋极锋利,堪称削铁如泥,吹毛断发。
仔细阅读上面文字,完成下面问题:
(1)青铜是金属材料中 要成分是 号);
(2)从文中信息可以看出,青铜具有
(3)吴王夫差剑表面的蓝色薄锈,其主要成分为碱式碳酸铜[化学式:Cu2(OH)2CO3],这层蓝色薄锈形成的可能原因是
查看答案和解析>>
科目:初中化学 来源: 题型:
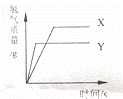
现有等质量X,Y的两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X,Y在生成物中化合价均为+2价).则下列说法不正确的是()
|
| A. | 生成氢气的质量:X>Y | B. | 相对原子的质量:X>Y |
|
| C. | 金属活动性:X>Y | D. | 消耗硫酸的质量:X>Y |
查看答案和解析>>
科目:初中化学 来源: 题型:
金属材料在国防建设中起着重要的作用,图1为歼﹣15飞机在辽宁舰上起飞.
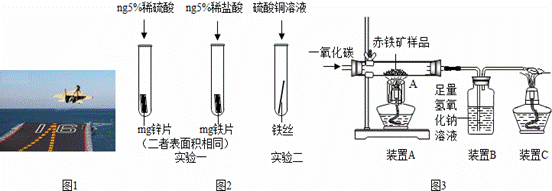
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是 、 .
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的 共同作用的结果.工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为 .
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属.小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是 .
②实验二中,若出现 现象,可证明铁的活动性强于铜,该反应的化学方程式为
(4)辽宁舰的建造耗费了大量的钢材.某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称重赤铁矿样品的质量为wg).
①装置A中生成铁的化学方程式为 ,装置B中发生反应的化学方程式为 .
②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
下表为两种物质在不同温度时的溶解度
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
|
| 溶解度/g | KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
请回答:
(1)60℃时,KCl的溶解度是 g;
(2)40℃时,将30g KCl加入到50g水中,充分溶解后所得溶液是 溶液(填写“饱和”或“不饱和”);
(3)将20℃时KNO3和KCl的两种饱和溶液升温至60℃,则两种溶液的溶质质量分数大小关系是:KNO3 KCl(填写“>”、“<”或“=”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com