
| A. | 浮有冰的水 | B. | 矿泉水 | C. | 自来水 | D. | 硬水 |
科目:初中化学 来源: 题型:选择题
| A. | 同种元素的原子和离子质子数相同 | |
| B. | 原子的最外层电子数与元素的化学性质密切相关 | |
| C. | 最外层电子数相同的粒子一定是同一种原子 | |
| D. | 质子数与核电荷数都可决定原子种类 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
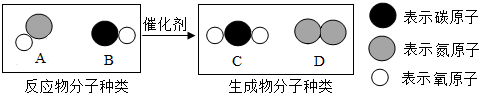
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
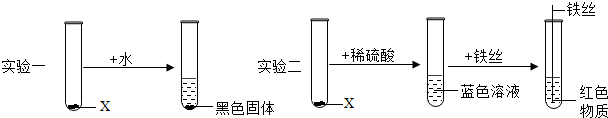
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 纯净物-④⑤⑥ | B. | 混合物-②③⑥ | C. | 碱-①⑤ | D. | 盐-③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 操作步骤 | 现象记录 | 反应的化学方程式 |
| 取两支试管,分别往试管中加入2mL样品,再往其中滴入盐酸 | 样品1:无明显现象 | NaOH+HCl=NaCl+H2O |
| 样品2:溶液中出现气泡 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ |

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com