
| ||
| ||


科目:初中化学 来源: 题型:
| A、甲同学说:该条件下NaHCO3的溶解度较大 |
| B、乙同学说:NaHCO3不是纯碱 |
| C、丙同学说:析出NaHCO3固体后的溶液为碳酸氢钠的饱和溶液 |
| D、丁同学说:从该反应可以获得氮肥 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
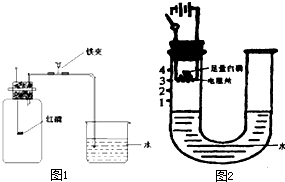 在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.已知红磷和白磷的化学性质相似,二氧化硫能与氢氧化钠溶液反应生成亚硫酸钠固体和水,亚硫酸钠固体能溶于水.(实验装置如图1所示)回答下列问题:
在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.已知红磷和白磷的化学性质相似,二氧化硫能与氢氧化钠溶液反应生成亚硫酸钠固体和水,亚硫酸钠固体能溶于水.(实验装置如图1所示)回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com