
【题目】农业上常用溶质质量分数为16%的氯化钠溶液来选种。某兴趣小组用纯净的氯化钠固体来配制16%的氯化钠溶液,请你回答下列问题:
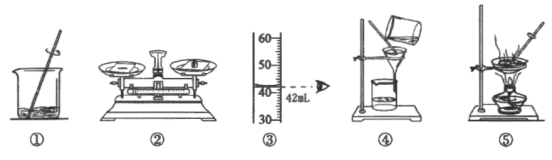
(1)实验中不需要的操作步骤_____(填序号)。
(2)若按如图所示要求配制氯化钠溶液,需要氯化钠的质量为_____g。
(3)实验后测得溶质质量分数<16%,其原因可能是_____。(一种即可)
(4)室温下氯化钠的溶解度约为36g。若要将配制的溶液转化为该温度下的饱和溶液,较简单的方法是_____。
【答案】④⑤ 8 少量固体残留在称量纸上 向溶液中再加入7.1g氯化钠固体并充分搅拌
【解析】
(1)纯净的氯化钠固体来配制16%的氯化钠溶液主要步骤是计算、称取、量取和溶解,实验中不需要的操作步骤过滤和蒸发,故选④⑤;
(2)设:需要氯化钠的质量x。![]() x=8g。若按如图所示要求配制氯化钠溶液,需要氯化钠的质量为8g;
x=8g。若按如图所示要求配制氯化钠溶液,需要氯化钠的质量为8g;
(3)如果配制的氯化钠溶液的实际浓度小于16%,称量氯化钠时操作错误如:用到了游码且氯化钠和砝码放反了;天平未调零等;少量固体残留在称量纸上;用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小;其它如氯化钠中含有杂质;烧杯中有水等;
(4)设:室温下质量为y的氯化钠与42g的水形成饱和溶液。根据溶解度概念则有:![]() y=15.1g,所以若要将配制的溶液转化为该温度下的饱和溶液,需再加入15.1g-8g=7.1g的氯化钠。若要将配制的溶液转化为该温度下的饱和溶液,较简单的方法是向溶液中再加入7.1g氯化钠固体并充分搅拌。
y=15.1g,所以若要将配制的溶液转化为该温度下的饱和溶液,需再加入15.1g-8g=7.1g的氯化钠。若要将配制的溶液转化为该温度下的饱和溶液,较简单的方法是向溶液中再加入7.1g氯化钠固体并充分搅拌。


 名师点拨卷系列答案
名师点拨卷系列答案科目:初中化学 来源: 题型:
【题目】在t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如右图甲所示,硝酸钾和氯化钾的溶解度曲线如右图乙所示。下列说法错误的是( )
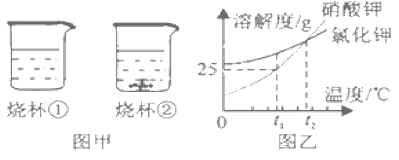
A. 烧杯②中的上层溶液是饱和溶液
B. 烧杯①中溶液的溶质是硝酸钾
C. 烧杯①中溶液质量比烧杯②中溶液质量小
D. 将温度升高到t2℃,烧杯②中的固体全部溶解
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示,关于该转化关系图,下列说法正确的是( )
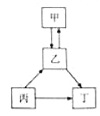
A.如果丙是碳酸钠,乙是氢氧化钠,则甲是硝酸钠
B.若甲、乙、丁都是氧化物,则丙一定是碳酸钙
C.甲、乙、丙、丁之间的转化可以全部通过复分解反应实现
D.若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火,则丙一定是单质碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】广陵区“8424”西瓜美誉全城,西瓜可解暑、止渴,如图列出了西瓜的营养成分。
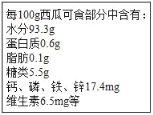
(1)西瓜具有甜味,主要是因为含有_____的原因,西瓜可食部分中含量最多的物质是_____;
(2)“钙、磷、铁、锌17.4mg”是指_____(填“单质”或“元素”)的质量,其中不属于人体微量元素的是_____;缺铁元素可致_____,缺_____元素可引起儿童发育停滞,智力低下,严重可导致侏儒症;
(3)检验某种食物中是否含有淀粉可选用_____(填试剂名称)滴在食物样品上,观察是否变_____色。
(4)糖类在人体内转化为葡萄糖后,再经过_____向人体提供能量(填“呼吸作用”或“光合作用”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,KCl 的溶解度为 34.0g。向下列 4 只盛有 100g 水的烧杯中,分别加入不同质量的 KCl 固体,充分溶解。下列说法不正确的是
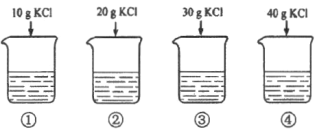
A. 上述溶液为不饱和溶液的是①②③B. 有固体残留的烧杯是③④
C. ②溶液中溶质的质量分数为 16.7%D. ①溶液中再加入 24.0g 固体恰好饱和
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有A、B、C三种元素,它们形成的粒子结构示意图如下,其中说法正确的是( )
元素 | A | B | C |
其形成的粒子结构示意图 |
|
|
|
A. 它们之间可形成化学式为AC的化合物
B. 它们原子的核外电子层数相同
C. A的粒子结构示意图表示的是原子, B、C表示的是阳离子
D. 它们之间可形成化学式为B2A的化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在用白磷(白磷与红磷组成相同,着火点为40℃)探究质量守恒定律的实验中,晓涵同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如下图所示。请回答下列问题:
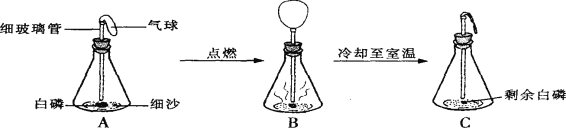
(1)实验观察到A、C中气球的大小不同,产生此现象的原因是 __________________;B气球胀大的原因是:_______________________。
(2)装置:锥形瓶的底部铺有一层细沙,其作用是 ________________;气球的作用是:_______。
(3)白磷燃烧:白磷燃烧过程中看到的现象是 ________ 。
(4)反思:白磷燃烧 _____(填“遵守”或“不遵守”)质量守恒定律,理由是 ______________ ;该反应的方程式:______________,该反应的基本类型为_____________,
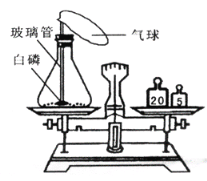
(5)燃烧前称量,锥形瓶的总质量为29.6g,则右图托盘天平中游码的读数为________g.
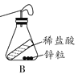
(6)某同学用 图B 所示的装置测定质量守恒定律,将锌粒和稀盐酸混合后称量:发现托盘天平指针偏向右边,造成的原因可能是 _____________(只写一条)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】汽车作为一种常见交通工具,已走进千家万户.请回答下列问题:
(1)目前汽车使用的燃料是汽油.将石油加热,利用各成分的沸点不同将它们分离可得到汽油,该过程
属于___变化.
(2)我国已推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇,作为汽车的燃料.下列叙述正确的是___.
A 乙醇汽油是一种新型的化合物 B 乙醇可通过粮食发酵的方法制得
C 使用乙醇汽油能减少有害气体的排放 D 乙醇和汽油都是可再生能源
(3)乙醇俗称酒精,他在空气中完全燃烧生成二氧化碳和水,该反应的化学方程式为:___.
(4)汽车生产过程汇总需要各种金属,其中用量最大的是金属铁.
①生活中接触到“加铁酱油”,这里的铁指的是___.
A 元素 B 分子 C 原子 D 单质
②高铁酸钠(Na2FeO4)是一种新型的高效的净水剂,高铁酸钠中铁元素的化合价为___.
③常见的食品脱氧剂多为无机铁系脱氧剂,请将下列脱氧中的主要反应的化学方程式补充完成4Fe(OH)2+O2+2___═4Fe(OH)3; 此反应的基本类型是___.
④工业上炼铁的简要流程如下:(赤铁矿的主要成分是氧化铁)

请写出步骤Ⅱ、步骤Ⅲ的化学反应方程式:Ⅱ___;Ⅲ___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从2012年中国第一艘航母“辽宁舰”入列到2018年第三艘航母在建,标志着中国海军从此迈入航母时代和海军发展强国,开拓中国新蓝海。

(1)“航母”舰体材料为合金钢。国产航母使用的“超级钢”具有极佳的抗压性、延展性和焊接性。合金钢是_____(填字母)。
a合成材料
b复合材料
c金属材料
(2)“航母”升降机可由铝合金制造。用石墨作电极在高温条件下电解熔融氧化铝,在阴极和阳极区分别得到Al和O2,阳极区使用的石墨易消耗的原因是_____。
(3)“航母”螺旋桨可由铜合金制造。铜合金比铜的硬度_____(填“大”或“小”),铜比铁在海水中耐腐蚀的原因是_____。
(4)“航母”船体需做特殊防锈处理才能耐腐蚀。请写出生活中防止钢铁生锈的一种方法:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com