
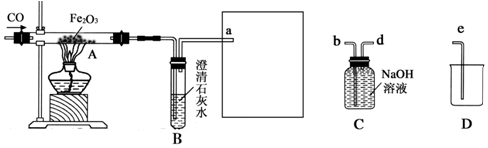
分析 (1)根据氢氧化钠溶液能吸收二氧化碳,用排液体收集气体的方法;
(2)根据一氧化碳易可燃,容易发生爆炸考虑;
(3)根据化学反应的原理和化学方程式的书写方法考虑.
解答 解:(1)一氧化碳有毒,不能够排放到空气中去,要把一氧化碳收集起来,所以导管接口的连接顺序为a、d、b、e,排出的氢氧化钠溶液流到D中的烧杯中去.C装置中NaOH的作用是吸收B中没反应掉的二氧化碳;
(2)因为一氧化碳具有可燃性,能和氧气混合在点燃的条件下会发生爆炸,所以实验开始时应先通一氧化碳再加热,目的是赶尽玻璃管内的空气,防止加热爆炸;
(3)二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水;
故答案为:(1)d;b;(2)先通CO再加热;(3)CO2+Ca(OH)2═CaCO3↓+H2O.
点评 本题主要考查一氧化碳与氧化铁反应实验装置、实验现象、一氧化碳的化学性质和污染及能源的再利用,难度稍大.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
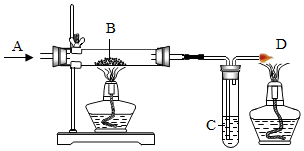 小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.
小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.| 序号 | 探究实验 | 简答 |
| Ⅰ | 若为H2与CuO的反应 | B处玻璃管观察到现象:出现水珠. |
| Ⅱ | 若为CO与CuO的反应 | B处反应的化学方程式:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2, 发生氧化反应的物质是:CO. |
| Ⅲ | 若为CO2与C 的反应 (B处换成酒精喷灯加热) | B处的黑色粉末逐渐减少,最后消失, D处观察到有蓝色的火焰. |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | A2B | B. | A2B3 | C. | AB2 | D. | A3B2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
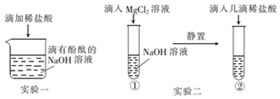 实验小组在探究“酸与碱能否发生反应”时,进行了如图所示实验.请根据实验回答:
实验小组在探究“酸与碱能否发生反应”时,进行了如图所示实验.请根据实验回答:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 分别用带火星的木条伸入气体中 | B. | 观察颜色、状态、闻气味 | ||
| C. | 分别用吹肥皂泡的方法 | D. | 通电电解后利用电极来判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com