
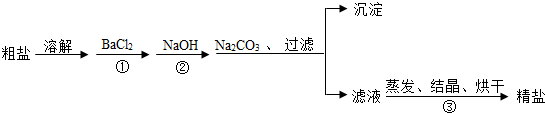
分析 (1)根据除杂质的同时不能引入新杂质进行解答;
(2)根据要除去杂质,需加入过量的除杂物质,要判断BaCl2是否过量,可取少量上层清液,继续滴加BaCl2溶液,观察现象进行解答;
(3)根据在②步后,溶液中存在的物质有:未反应的氯化钡、氯化钙,要将钡离子和钙离子除去,可加入碳酸钠进行解答;
(4)根据过滤前的溶液中加入的碳酸钠和氢氧化钠都是过量的,反应后两者都有剩余进行解答.
解答 解:(1)在除杂质的同时不能引入新的杂质,加入硝酸钡会生成新的杂质硝酸钠,这样会在溶液中引入硝酸根离子.
(2)要除去杂质,需加入过量的除杂物质,要判断BaCl2是否过量,可取少量上层清液,继续滴加BaCl2溶液,如没有白色沉淀出现,则说明BaCl2过量;
(3)在②步后,溶液中存在的物质有:未反应的氯化钡、氯化钙,要将钡离子和钙离子除去,但是不能引入新的杂质,所以加入碳酸钠;
(4)过滤后滤液的主要成分有:NaCl、NaOH、Na2CO3,所以按该实验方案制得的精盐并不纯净,其中含有的杂质是氢氧化钠、碳酸钠.
故答案为:
(1)会引入无法除去的杂质离子NO3-.
(2)在上层清液中继续滴加BaCl2溶液,若无沉淀出现,则BaCl2过量,反之未过量.
(3)Ca2+、Ba2+.
(4)氢氧化钠、碳酸钠.
点评 本题主要考查了粗盐提纯实验的过程,及除杂原则:在除去杂质的同时不能引入新的杂质,通过本题能很好的考查学生严密思考,分析、解决问题的能力.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | H2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 与水任意比互溶 | 19.0 | 39.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 用浓硫酸在白纸上写字 | 白纸变黑甚至穿孔 | 浓硫酸有强烈的腐蚀性 |
| B | 向稀盐酸中加入氢氧化钠溶液 | 无明显现象 | 二者之间不发生反应 |
| C | 在装有过氧化氢溶液的试管中加入MnO2固体 | 有大量气泡产生 | MnO2是过氧化氢溶液 分解的催化剂 |
| D | 向某溶液滴加BaCl2溶液,振荡 | 有白色沉淀生成 | 该溶液一定含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 事 实 | 解 释 |
| A | 氧化汞受热会得到氧气和汞 | 分子在化学变化中可以再分 |
| B | 盐酸、稀硫酸都能使紫色石蕊试液变红 | 它们所含的阳离子全部都是H+ |
| C | 将墨汁滴入一杯清水中,清水很快变黑 | 分子在不断运动 |
| D | 25m3的氧气可以装入0.024m3的钢瓶中 | 氧分子的体积变小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com