
 了解溶液的酸碱度具有重要的意义.
了解溶液的酸碱度具有重要的意义.| 血浆 | 7.35-7.45 |
| 胃液 | 0.9-1.5 |
| 胰液 | 7.5-8.0 |
| 尿液 | 4.7-8.4 |
分析 (1)根据溶液的酸碱度具体测定方法是用干燥的玻璃棒蘸取(或胶头滴管吸取)少量的待测溶液,并滴在放在干燥的玻璃皿或白瓷板上的干燥pH试纸上,再把试纸显示的颜色与标准比色卡比较,即可得出待测溶液的pH解答;
(2)根据二氧化碳和水反应生成碳酸解答;
(3)根据酸性溶液,pH越小,酸性越强解答;
(4)根据氢氧化钠与盐酸恰好完全反应时溶液呈中性分析;
解答 解:
(1)测定溶液酸碱度的方法:用干燥的玻璃棒蘸取(或胶头滴管吸取)少量的待测溶液,并滴在放在干燥的玻璃皿或白瓷板上的干燥pH试纸上,再把试纸显示的颜色与标准比色卡比较,即可得出待测溶液的pH;
(2)正常雨水的pH约为5.6的主要原因是二氧化碳和水反应生成碳酸,化学方程式表示为:H2O+CO2=H2CO3
(3)酸性溶液,pH越小,酸性越强,酸性最强的是胃液;
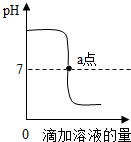
(4)此时溶液的pH值等于7,氢氧化钠与盐酸恰好完全反应时溶液呈中性,图中a点对应溶液所含的溶质是氯化钠;
答案:
(1)取一小片 pH试纸放在玻璃片(或白板)上,用玻璃棒蘸取待测液滴在pH试纸上,与标准比色卡对照,读出溶液的pH
(2)H2O+CO2=H2CO3
(3)胃液
(4)NaCl
点评 本题难度不大,掌握溶液酸碱性、酸碱度的测定方法、了解pH试纸检验溶液的酸碱度的方法可正确解答本题.


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:初中化学 来源: 题型:解答题
| 实验编号 | 铝铜合金的质量(g) | 加入稀硫酸的质量(g) | 生成H2的质量(g) |
| 实验1 | 30 | 392 | 2 |
| 实验2 | 30 | 588 | 3 |
| 实验3 | 30 | 600 | 3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 22 | B. | 26 | C. | 58 | D. | 48 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 为治理雾霾,禁止使用化石燃料 | |
| B. | 变废为宝,将地沟油转化为航空燃油 | |
| C. | 城市道路使用太阳能景观灯,节能又环保 | |
| D. | 用二氧化碳和水等合成新型燃油,有利于减缓温室效应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
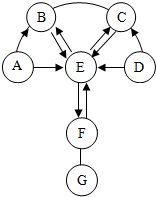 如图所示,A~G是初中化学常见的七种物质.图中“→”表示转化关系.“-”表示相互能反应.F可以用于改良酸性土壤,D、E组成元素相同,B、C、G常温下为气体,在实验室中常用A制取G.
如图所示,A~G是初中化学常见的七种物质.图中“→”表示转化关系.“-”表示相互能反应.F可以用于改良酸性土壤,D、E组成元素相同,B、C、G常温下为气体,在实验室中常用A制取G.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )| A. | t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c | |
| B. | t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水) | |
| C. | t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是b>a=c | |
| D. | 将c的饱和溶液变为不饱和溶液,可采用降温的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题

| A. | 铝矾石中只含有金属氧化物 | |
| B. | 原料A可能是稀硫酸;滤液Ⅰ中要加入稍过量的原料B,原料B可能是氢氧化钠 | |
| C. | 步骤②所得沉淀是氢氧化亚铁 | |
| D. | 铝矾石炼铝需要消耗电能 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com