
 寒假学与练系列答案
寒假学与练系列答案科目:初中化学 来源: 题型:阅读理解
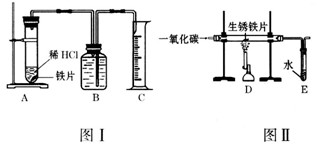
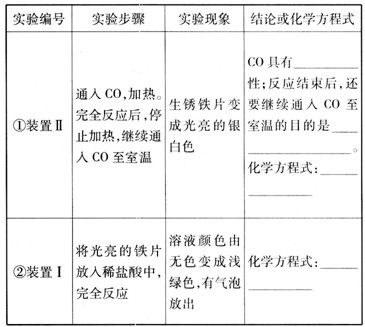
| 实验编号 | 实验步骤 | 实验现象 | 结论或化学方程式 |
① 装置Ⅱ |
通入CO,加热.完全反应后,停止加热,继续通CO至室温 | 生锈铁片变成光亮的银白色 |
CO具有 化学方程式: |
| ② 装置Ⅰ |
将光亮铁片放入稀盐酸中,完全反应 | 溶液颜色由无色变成浅绿色,有气泡放出 | 化学方程式: |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

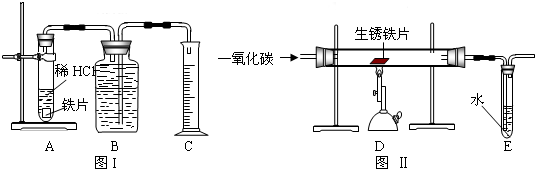
| 实验编号 | 实验步骤 | 实验现象 | 解释或化学方程式 |
①装置Ⅱ |
通入CO,加热.完全反应后,停止加热,继续通CO至室温 | 生锈铁片变成光亮的银白色 | 反应结束后,还要继续通CO至室温的目的是 防止铁片在高温下又被氧化或防止倒吸 防止铁片在高温下又被氧化或防止倒吸 . |
| ②装置Ⅰ | 将光亮铁片放入稀盐酸中,完全反应 | 溶液颜色由无色变成浅绿色,有气泡放出 | 化学方程式: Fe+2HCl═FeCl2+H2↑ Fe+2HCl═FeCl2+H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
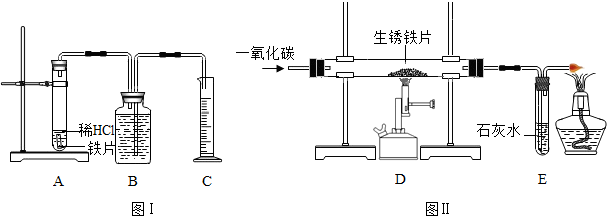
| 试验编号 | 实验步骤 | 实验现象 | 结论或化学方程式 | ||||||||
| ①装置II | 通入CO加热,完全反应后,停止加热,继续通入CO至室温 | 生锈铁片变成光亮的银白色 | CO具有 还原 还原 性,化学方程式为Fe2O3+3CO
Fe2O3+3CO
| ||||||||
| ②装置I | 将光亮铁片放入稀盐酸中,完全反应 | 溶液颜色由无色变成浅绿色,有气泡放出 | 化学方程式为 Fe+2HCl═FeCl2+H2↑ Fe+2HCl═FeCl2+H2↑ |
| 2800ρ1v2 |
| m2 |
| 2800ρ1v2 |
| m2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
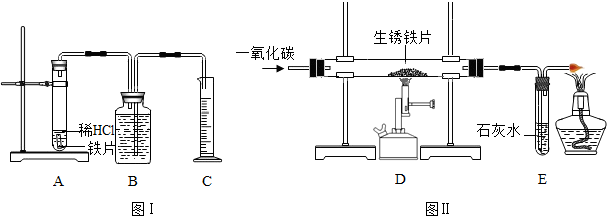
| 试验编号 | 实验步骤 | 实验现象 | 结论或化学方程式 |
| ①装置II | 通入CO加热,完全反应后,停止加热,继续通入CO至室温 | 生锈铁片变成光亮的银白色 | CO具有________性,化学方程式为________ |
| ②装置I | 将光亮铁片放入稀盐酸中,完全反应 | 溶液颜色由无色变成浅绿色,有气泡放出 | 化学方程式为 ________ |
查看答案和解析>>
科目:初中化学 来源:2009年四川省成都市中考化学试卷(解析版) 题型:解答题
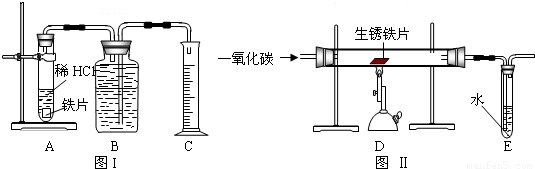
| 实验编号 | 实验步骤 | 实验现象 | 结论或化学方程式 |
① 装置Ⅱ | 通入CO,加热.完全反应后,停止加热,继续通CO至室温 | 生锈铁片变成光亮的银白色 | CO具有______性;反应结束后,还要继续通CO至室温的目的是______ 化学方程式:______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com