
| 药品、实验编号 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
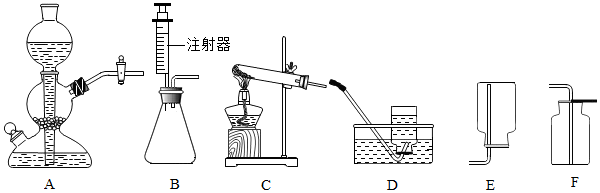
| 目的 | 原料 | 发生装置 | 气体比较平稳产生的最主要一个原因 |
| 制取二氧化碳 | 块状大理石 稀盐酸 | A | |
| 制取氧气 | 粉末状二氧化锰 3%的过氧化氢溶液 | B |
分析 (1)据反应原理书写方程式;
(2)氧气可用向上排空气法收集是因为氧气密度比空气大,且不与空气中成分发生反应;排水法收集满的现象是集气瓶口有大气泡冒出;
(3)用氯化铵固体和碱石灰固体共热来制取氨气,属于固体加热型,故选发生装置C,并据氨气密度和溶解性选择收集装置;
(4)①大理石的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水和二氧化碳;
②根据控制变量法分析解答;
③根据实验数据、物质状态分析解答;
④从反应物之间的接触面积和注射器的特点来分析.
解答 解:(1)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)氧气可用向上排空气法收集是因为氧气密度比空气大,且不与空气中成分发生反应;排水法收集满的现象是集气瓶口有大气泡冒出;
(3)用氯化铵固体和碱石灰固体共热来制取氨气,属于固体加热型,故选发生装置C,氨气密度比空气小,极易溶于水,所以只能用向下排空气法收集;
(4)①大理石主要成分碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳反应方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②对比实验数据可见,甲和乙均为mg块状大理石,wg盐酸,但是盐酸的浓度不同,故填:乙;
③甲和丙对比,乙和丁对比可知,实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积);
④用块状大理石与稀盐酸反应来较平稳的产生二氧化碳,是因为块状大理石与稀盐酸的接触面积较小;用过氧化氢来制取氧气时,用注射器滴加过氧化氢溶液,这样就可以控制液体滴加的速度,从而得到了较平稳的氧气流;
故答案为:(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)氧气的密度比空气大、不与空气中成分反应;集气瓶口有大气泡冒出;
(3)C;E;
(4)①②③固体反应物的颗粒大小(或反应物的接触面积);
④反应物的接触面积较小;通过注射器可控制液体滴加速度,进而可控制反应速率.
点评 本题考查了实验室制取气体 的装置选取、反应原理、以及对影响实验速率的因素的探究、控制变量法的应用等知识,要结合题意认真分析解答.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 据报道,全球每年浪费掉的粮食约有1000亿吨,其中约300亿吨是加工过的食品.如图所示是一包烤花生的图片,图中的脱氧剂在食品防腐保鲜,特别是对延长含高油脂食品的保质期有着重要作用.请回答下列问题:
据报道,全球每年浪费掉的粮食约有1000亿吨,其中约300亿吨是加工过的食品.如图所示是一包烤花生的图片,图中的脱氧剂在食品防腐保鲜,特别是对延长含高油脂食品的保质期有着重要作用.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硝酸铵溶于水吸收大量的热,食盐溶于水也吸收大量的热 | |
| B. | 氮肥氯化铵与碱研磨可放出氨气,氮肥尿素(CO(NH2)2)与碱研磨也能放出氨气 | |
| C. | 因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 | |
| D. | 氢气与空气混合点燃可能爆炸,一氧化碳与空气混合点燃也可能爆炸 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 化学是一门以实验为基础的科学,请回答下列有关实验问题:
化学是一门以实验为基础的科学,请回答下列有关实验问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学是一门富有创造性的科学.含氟物质的合成,对推动社会进步发挥着巨大作用.
化学是一门富有创造性的科学.含氟物质的合成,对推动社会进步发挥着巨大作用. ,由氟原子的结构示意图知,氟原子在化学反应中易得(填“失”或“得”)电子.
,由氟原子的结构示意图知,氟原子在化学反应中易得(填“失”或“得”)电子.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com