

| 猜想 | 实验步骤 | 现象与结论 |
| 此气体可能是(填化学式)O2 |
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据固体和液体接触反应生成气体,可能是过氧化氢与二氧化锰混合,检验氧气使用的是带火星的木条,氧气能使带火星的木条复燃,要收集氧气,可以依据氧气的密度和水溶性进行分析;
(3)根据实验室制取二氧化碳的反应物是石灰石和稀盐酸,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是酒精灯,②是集气瓶;
(2)固体和液体接触反应生成气体,可能是过氧化氢与二氧化锰混合,检验氧气使用的是带火星的木条,氧气能使带火星的木条复燃,所以:
| 猜想 | 实验方法 | 现象及结论 |
| 此气体可能是O2 | 将带火星的木条伸进试管内 | 木条复燃,该气体是氧气 |
| 猜想 | 实验方法 | 现象及结论 |
| O2 | 将带火星的木条伸进试管内 | 木条复燃,该气体是氧气 |
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
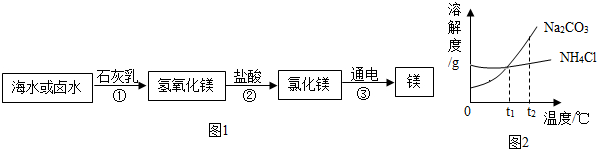
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
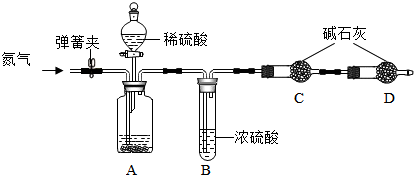
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 空气是一种十分重要的天然资源 | |
| B. | 少量有害气体进入空气中,依靠大自然的自净能力,空气仍能保持洁净 | |
| C. | 空气中的稀有气体一般不跟其他物质反应,曾被称为“惰性气体” | |
| D. | 按质量计算,空气中约含氮气78%,氧气21%,其他气体和杂质约占1% |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
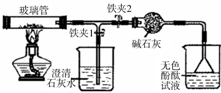
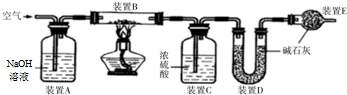
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com