
反应②是工业炼铁的主要原理,F为赤铁矿石的主要成分,A、C、E都是氧化物, D、G、I属于单质,下图是它们之间的相互转化关系。请回答:
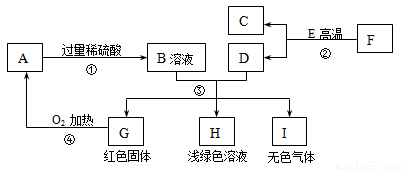
(1)B溶液中所含有的溶质为_______________,固体A的化学式为________,H溶液显浅绿色,其中所含有的溶质是________________。
(2)写出反应②的化学方程式________________________________。
(3)写出反应③的化学方程式________________、_______________。
(4)指出物质A和I在加热条件下发生的化学反应的基本反应类型______________。
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:2016届湖北省黄石市九年级上学期12月联考化学试卷(解析版) 题型:推断题
小明在化学实验室发现了一块绿色的孔雀石样品,他查阅资料后知道其成分为碱式碳酸铜[Cu2(OH)2CO3]。小明以孔雀石(不考虑其中的杂质参与反应)为原料设计了如下图所示(部分生成物略去)的化学反应,请回答下列问题:
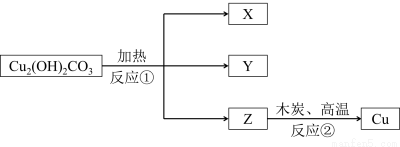
【已知】
a.碱式碳酸铜受热会分解成三种氧化物;
b.在反应①中各元素的化合价不变;
c.其中X是一种气体,Y是最常见的液态物质,Z是黑色固体。
(1)写出反应①的化学方程式____________________________________;在该反应的结束后,固体中铜元素的质量分数____________(填“变大”、“不变”或“变小”)。
(2)可用下图完成反应②的相关实验:
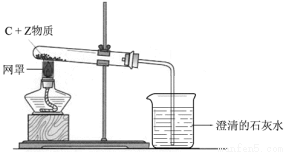
Ⅰ.写出该反应的化学方程式__________________,试管中的实验现象________________,其中网罩的作用是______________________。
Ⅱ.实验结束后,进行操作是_________。
a.先把导管从澄清石灰水中撤出,后熄灭酒精灯
b.先熄灭酒精灯,后把导管从澄清石灰水中撤出
查看答案和解析>>
科目:初中化学 来源:2016届山东省东营市九年级上学期12月月考化学试卷(解析版) 题型:选择题
某方程式为3C02 + 4Na = 2X + C。则x的化学式为:
A. Na2O2 B .Na4C2O6 C. Na2O D.Na2CO3
查看答案和解析>>
科目:初中化学 来源:2016届江苏省苏州市区九年级上学期期终调研测试化学试卷(解析版) 题型:选择题
微量元素是指在人体内总量不到万分之一的20多种元素,这些元素对人体正常代谢和健康起着重要作用,下列元素是微量元素是
A.氢 B.碳 C.铁 D.氧
查看答案和解析>>
科目:初中化学 来源:2016届江苏省泰州市姜堰区九年级上学期期末化学试卷(解析版) 题型:填空题
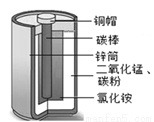
锌锰电池材料中含铜,构造如图。请回答下列问题:
(1)下列铜制品中,利用金属导热性的是 (填字母序号);
A.铜质奖牌 B.铜导线 C.铜火锅
(2)图中所示物质属于非金属单质的化学式是 ;
(3)氯化铵中氮元素的化合价是 ;
(4)电池铜帽为铜锌合金。某课外活动小组为测定铜帽中铜的质量分数,设计实验如下:
取铜帽样品10g放入烧杯,加入50g稀硫酸,恰好完全反应,烧杯内剩余物的总质量为59.8g。计算:
①产生氢气的质量为 g;
②样品中铜的质量分数;
③所用稀硫酸中溶质的质量分数(②、③写出计算过程)。
查看答案和解析>>
科目:初中化学 来源:2016届江苏省东部分校九年级上学期期末化学试卷(解析版) 题型:探究题
(一)如图是实验室常用气体制备装置,据图回答问题:
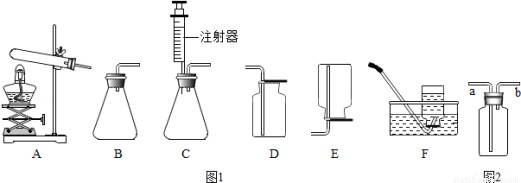
(1)实验室用高锰酸钾制氧气的化学方程式是 ,应选择的发生装置是 (填字母代号),为保证实验顺利进行,装置中还应添加 ,如果选用如图2装置收集氧气,气体应从 (填“a”或“b”)端导入,若瓶中装满水,则气体应从 端导入(填“a”或“b”);
(2)实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为 ,某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用B装置来制氧气。实验中,同学们发现不能得到平稳的氧气流。大家提出从两个方面加以改进:
一是把发生装置由B改为C,其理由是 ;
二是将过氧化氢溶液加水稀释,溶液的稀释须要经过计算,量取,搅匀三个步骤;
如把50g质量分数为20%的过氧化氢溶液稀释成5%的过氧化氢溶液,需加水的质量为 g,在稀释过程中,除了烧杯外,还需要用到的仪器有 (填数字序号);
①量筒 ②药匙 ③试管 ④酒精灯 ⑤滴管 ⑥玻璃棒
(3)兴趣小组的同学看到实验室里还有大理石,想利用图1中的C装置和 装置结合制备并收集一瓶二氧化碳,发生反应的方程式为 ,某同学用 来检验生成的二氧化碳,看到 ,发生反应的方程式为 。
(二)为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出)。
【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气。
②碱石灰为固体氢氧化钠和氢氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X。
③本实验条件下,氮气密度为1.15g•L﹣1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计。
【实验步骤】
①连接仪器,并检查装置气密性。
②取一定量氧化铜,准确称得其质量为2.40g。
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测得相关的量记录在数据Ⅰ(见表)。
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热。当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却后,再次测量并记录相关数据Ⅱ(见表)。
【实验装置】
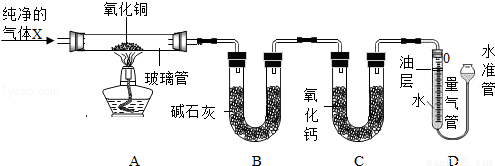
【相关数据】
测量项目/数据编号 | Ⅰ | Ⅱ |
玻璃管(含药品)的质量/g | 52.40 | 51.92 |
B装置(含药品)的质量/g | 102.00 | 102.54 |
氮气的体积/mL | / | 243.5 |
【回答问题】
(1)B中装置中氧化钙吸水的原理为 (用化学方程式表示);
(2)实验过程中,当观察到 ,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是 ;
(3)分析实验测量的数据,生成水的质量为 g,氧化铜中氧元素的质量为 g.由此推知,气体X中一定 (填“有”或“没有”)氧元素.
④读取量气管中氮气体积之前需要 ,通过计算推导出气体X的化学式为 。
查看答案和解析>>
科目:初中化学 来源:2016届江苏省镇江市九年级上学期期末考试化学试卷(解析版) 题型:填空题
FeSO4•7H2O是一种重要的食品和饲料添加剂。某工业废渣主要成分是Fe2O3,还含有CaCO3和SiO2(SiO2既不溶于水也不溶于稀硫酸)。实验室用此废渣制备FeSO4•7H2O的流程如图1:
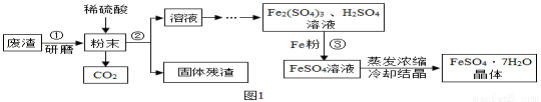
请根据流程图回答下列问题:
(1)步骤①研磨的目的是 。
(2)操作②的名称是 ,所需要的玻璃仪器是:烧杯、玻璃棒和 。
(3)经测定,固体残渣中只含有CaSO4和SiO2,你认为实验室 (填“能”或者“不能”)用粉末状的石灰石与稀硫酸反应制二氧化碳。
(4)写出③中发生的化学反应方程式 、 。
(5)已知硫酸亚铁的溶解度和析出晶体的组成如下表:
温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | |
析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
根据上表,硫酸亚铁晶体(FeSO4•7H2O)冷却结晶温度最高不超过 ;待结晶完毕后,滤出晶体,用少量冰水洗涤2﹣3次。用冰水洗涤的目的是:Ⅰ除去晶体表面附着的杂质;Ⅱ 。
查看答案和解析>>
科目:初中化学 来源:2016届山东省济南市商河县九年级上学期期末化学试卷(解析版) 题型:选择题
古语道:“人要实,火要虚”。此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺。从燃烧的条件看,“火要虚”的实质是( )。
A.增大可燃物的热值 B.提高空气中氧气的含量
C.提高可燃物的着火点 D.增大可燃物与空气的接触面积
查看答案和解析>>
科目:初中化学 来源:2016届山东省泰安市东平县九年级上学期期末化学试卷(解析版) 题型:选择题
(2015秋•东平县期末)如图所示是利用海水提取粗盐的过程:
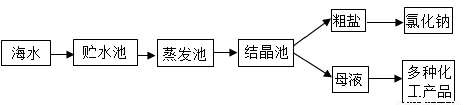
根据海水晒盐的原理,下列说法中:①海水进入贮水池,海水的成分基本不变②在蒸发池中,海水中氯化钠的质量逐渐增加③在蒸发池中,海水中水的质量逐渐增加④析出晶体后的母液是氯化钠的饱和溶液,正确的是( )
A.①③ B.②④ C.①④ D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com