
| A. | 碳酸钠的水溶液能使酚酞变红,所以碳酸钠属于碱 | |
| B. | 高锰酸钾中含有氧元素,所以高锰酸钾属于氧化物 | |
| C. | 水和双氧水的组成元素相同,所以它们的性质完全相同 | |
| D. | 水在通电条件下生成氢气和氧气,所以水是由氢、氧元素的组成的 |
分析 A、根据碳酸钠的分类解答;
B、根据氧化物是由两种元素组成并且一种元素是氧元素的化合物解答;
C、根据从水和双氧水分子构成不同,所以它们的化学性质不同去分析;
D、根据化学反应前后元素的中类不变解答.
解答 解:
A、碳酸钠的水溶液显碱性,能使酚酞变红,但碳酸钠属于盐,故错误;
B、高锰酸钾中含有钾元素、锰元素和氧元素,不属于氧化物.错误;
C、水和双氧水虽然组成元素相同,但由于它们的分子构成不同,所以它们的化学性质不同;故错误;
D、化学反应前后元素的中类不变,水通电条件下生成氢气和氧气,所以水是由氢、氧元素的组成的,正确.
答案:D
点评 本题考查化学的一种重要学习方法--类推法,属于易错题目,因而同学们对一些典型的概念、理论准确记忆,理解把握.


科目:初中化学 来源: 题型:选择题
| A. | 氯化钠 食盐 NaCl2 | B. | 碳酸氢钠 纯碱 NaHCO3 | ||
| C. | 氢氧化钙 熟石灰 CaO | D. | 氢氧化钠 火碱 NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
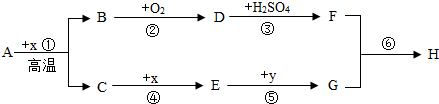
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
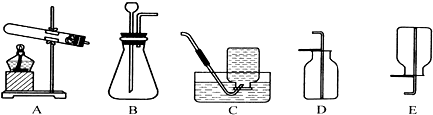
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在空气中剧烈燃烧,火星四射,放出大量的热,生产一种白色固体 | |
| B. | 向硫酸铜溶液中逐滴加入稀氢氧化钠溶液,可以观察到有蓝色沉淀生成 | |
| C. | 电解水实验中,与电源正极相连的玻璃管内生成的气体能使带火星的木条复燃 | |
| D. | 氨态氮肥与碱(氢氧化钠)混合加热,产生的气体能使湿润的红色石蕊试纸变蓝 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 所含杂质 | 除去方法 | 反应类型 |
| A | CuO粉 | Cu粉 | 在空气中加热 | 化合反应 |
| B | H2 | HCl | 通过盛氢氧化钠溶液的洗气瓶 | 分解反应 |
| C | CO2 | CO | 通过灼热的CuO | 置换反应 |
| D | NaCl | Na2SO4 | 溶解,加过量的氯化钡溶液,并过滤 | 复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com