
【题目】菠菜营养丰富,素有“蔬菜之王”的美称.民间流传:菠菜豆腐同食,易得结石.某化学兴趣小组对“菠菜豆腐是否不能同食”等问题进行了探究.
(查阅资料)①菠菜含有丰富的铁、草酸盐、碳酸盐等,豆腐中含有丰富的蛋白质及钙盐. ②人体结石的主要成分:草酸钙(CaC2O4) ③醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐等.
(提出猜想)“菠菜豆腐不能同食”的原因可能是:(1)_____
(探究一)菠菜中部分成分分析
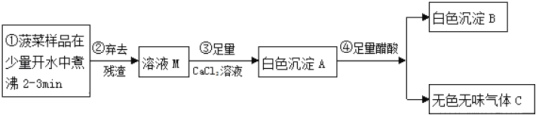
(2)步骤③中加入足量的CaCl2溶液的目的是添加_____离子.
(3)已知气体C能使澄清石灰水变浑浊,醋酸的化学式用HAC表示,写出步骤④的化学反应方程式_____.沉淀A、B的质量关系为:m(A)_____m(B)(填“>”、“<”或“=”).
(4)白色沉淀B的化学式为_____,由此可见菠菜豆腐不能同食.
(5)以下饮食观点正确的是_____(填序号)
A 禁吃菠菜 B 高钙牛奶可与菠菜同食C 菠菜烹饪时可用开水烫,降低草酸盐含量.
【答案】菠菜中的物质与豆腐中含有的钙离子反应产生不溶性物质 将菠菜中的草酸根离子、碳酸根离子完全转化为沉淀 CaCO3+2HAc═CaAc2+H2O+CO2↑; > CaC2O4 C
【解析】
(1)因菠菜含有草酸盐、碳酸盐,豆腐中含有钙盐,能反应生成沉淀,则不能同食,故答案为:菠菜中的物质与豆腐中含有的钙离子反应产生不溶性物质;
(2)因足量的CaCl2溶液可将菠菜中的草酸根离子及碳酸根离子充分反应;
(3)因气体C能使澄清石灰水变浑浊,则C为二氧化碳,根据信息醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐,则加醋酸时碳酸钙和醋酸反应生成了二氧化碳,化学反应方程式:CaCO3+2HAc═CaAc2+H2O+CO2↑,沉淀A为草酸钙和碳酸钙的混合物,而沉淀B为草酸钙;
(4)因加足量醋酸,碳酸钙完全反应,沉淀B中只有草酸钙,化学式为:CaC2O4;
(5)根据菠菜豆腐不能同食的观点,不吃菠菜是极端的,不科学的,高钙牛奶中的钙离子和菠菜中的离子反应,不能同食,而菠菜烹饪时可用开水烫,可降低草酸盐含量是正确的,。


科目:初中化学 来源: 题型:
【题目】某化学活动小组合作学习氢氧化钠和氢氧化钙的相关知识。如表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
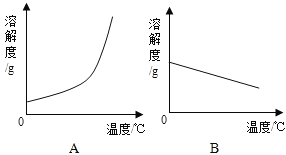
(1)依据上表数据,绘制了Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是_____(填“A”或“B”)。
(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入适量氢氧化钙②升高温度③降低温度④加入水⑤蒸发水后再恢复到原温度⑥加入适量生石灰。
其中措施在原理上正确的是_____(填字母)
A ②④⑥ B ③④ C ①②⑤⑥ D ①②⑤
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体。这时溶液的质量分数为_____
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH_____(填“偏大”或“偏小”“不受影响”)。
(5)可鉴别氢氧化钠溶液和澄清石灰水的一个化学反应方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室部分仪器或装置如图所示,请回答下列问题:
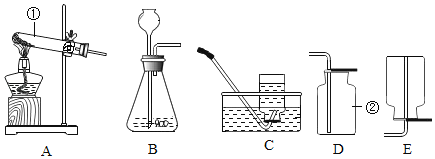
(1)标号①②的仪器名称:①_____②_____
(2)实验室常温下用过氧化氢溶液和二氧化锰的混合物制取氧气,其发生装置和收集装置的组合为_____,反应的文字表达式为_____。
(3)用B装置制取氧气时,反应速率比较快,可能导致实验变得不安全,你准备采用的改进措施是_____
(4)实验室选择AC装置制取氧气,反应的文字表达式为_____,收集完氧气后,应进行的操作是_____。(填①先撤离导管,再熄灭酒精灯或者②先熄灭酒精灯,再撤离导管。)理由是_____,若用C装置收集的氧气不纯,原因可能是_____(写一种即可),验满的方法是_____
(5)用收集到的氧气做细铁丝燃烧的实验:
①铁丝为什么要绕成螺旋状?_____
②集气瓶内为什么要预先装少量水或铺一层细沙?_____
③铁丝在氧气中燃烧的文字表达式_____
(6)已知甲烷是一种无色无味、密度比空气小,难溶于水的气体,实验室常用加热无水醋酸钠与碱石灰的固体混合物来制取甲烷,则实验室制取并收集甲烷选择的装置组合为_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】由以下粒子结构示意图得出的结论错误的是( )
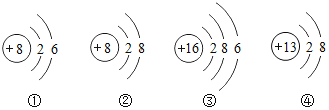
A. ④表示的阳离子
B. ③表示的元素位于元素周期表第六周期
C. ②④形成的化合物是A12O3
D. ①②属于同种元素,①③化学性质相似
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲乙丙三种物质均含地壳中含量最多的元素。甲乙是组成元素相同的化合物,丙是单质,甲、乙在常温下均为液体,在一定条件下均可分解生成丙;它们之间有如右图所示的转化关系(部分物质和反应条件已经略)。则甲物质的名称为_____;许多实验中都用到乙,写出乙在某一个具体实验中的作用_____。
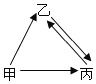
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】银杏果中含有银杏酸(化学式为C22H34O3),下列有关银杏酸说法正确的是
A. 银杏酸分子由碳、氢、氧三种元素组成
B. 银杏酸由22个碳原子、34个氢原子和3个氧原子构成
C. 银杏酸属于有机化合物
D. 银杏酸中氢元素的质量分数最大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铜、铁是人类使用最早、应用广泛的金属。
(探究一)
(1)铁生锈主要跟空气中的______有关,用稀硫酸除铁锈的化学方程式为________。
(2)小茜同学发现自己的铜制眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称“铜绿”,主要成分为Cu2(OH)2CO3,该反应的化学方程式为:2Cu+O2+H2O+X = Cu2(OH)2CO3,则X的化学式为__________。
(探究二)
以黄铜矿(CuFeS2)为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4![]() 4CuSO4+2Fe2(SO4)3+2H2O,向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu。
4CuSO4+2Fe2(SO4)3+2H2O,向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu。
(3)CuFeS2为二硫化亚铁铜,也可以表示为CuSFeS,其中S元素的化合价为_____。
(4)发生主要反应的两个化学方程式为:①Fe+Fe2(SO4)3=3FeSO4; ②_________。
(5)FeSO4溶液经蒸发浓缩、_______、过滤等操作得到硫酸亚铁晶体(FeSO4xH2O)。
(探究三)
硫酸亚铁晶体(FeSO4xH2O)是一种重要的食品和饲料添加剂,对其进行热分解研究。
(查阅资料)①硫酸铜粉末为白色,吸水后变成蓝色晶体。
②二氧化硫能使高锰酸钾溶液褪色
③硫酸亚铁晶体加热会先失去结晶水,高温会继续分解产生一种金属氧化物和两种非金属氧化物。
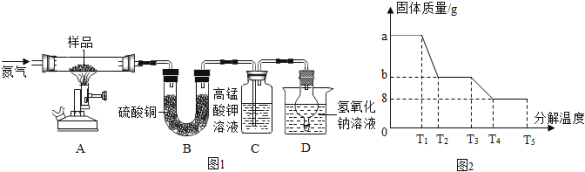
称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B的质量测出x的值。
(6)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有_______,装置C中高锰酸钾溶液褪色,说明产物中还有_________;装置D球形干燥管的作用_____;实验中要持续通入氮气,否则测出的x会_________(填“偏大”、“偏小”或“不变”)。
(7)硫酸亚铁晶体完全分解后,装置A中残留红棕色固体,另从理论上分析得出硫酸亚铁分解还生成另一物质SO3,写出FeSO4分解的化学方程式_______。
(8)某研究所利用热分析仪对硫酸亚铁晶体(FeSO4xH2O)进行热分解,获得相关数据,绘制成固体质量——分解温度的关系图如图2,根据图2中有关数据,可计算出FeSO4xH2O中的x=______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸铵((NH4)2SO4)是一种常用的化肥,它为农作物补充生长所需的氮元素。请根据化学式回答下列问题:
(1)硫酸铵由_____种元素组成,其中氮元素的化合价是_____;
(2)计算硫酸铵的相对分子质量_____(要有必要的过程,下同);
(3)计算硫酸铵中各元素的质量比_____;
(4)计算硫酸铵中氮元素的质量分数_____(保留一位小数);
(5)若今年种植玉米需要补充氮元素42.4千克,约需要硫酸铵多少千克_____?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置,回答问题:
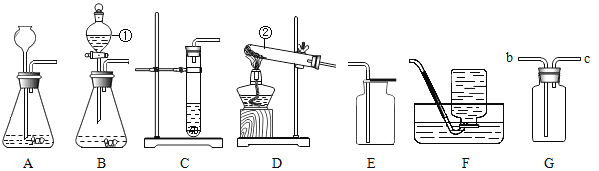
(1)写出图中标号仪器的名称:①_____;②_____。
(2)实验室利用下述发生装置制备氧气,其原理对环境较友好的化学反应化学式表达式是_____,发生装置最好选用_____(填装置序号)。优点是_____。
(3)采用加热高锰酸钾制取氧气时,反应的化学式表达式为_____,若收集较纯的氧气,可选用的收集装置是_____,若用G装置采用排空气法收集氧气,验满时,应将_____。若用G装置采用排空气法收集氢气,氢气应从_____进。(选“b”或“c”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com