
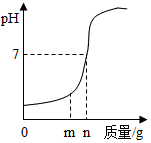
 用氢氧化钠中和一定量的盐酸时,溶液的pH与加入的氢氧化钠质量的关系如图所示:
用氢氧化钠中和一定量的盐酸时,溶液的pH与加入的氢氧化钠质量的关系如图所示:分析 稀盐酸和氢氧化钠反应生成氯化钠和水,和氢氧化钙反应生成氯化钙和水.
解答 解:(1)当加入的氢氧化钠为mg时,稀盐酸过量,溶液中的溶质为反应生成的氯化钠和过量的氯化氢.
故填:NaCl、HCl.
(2)氢氧化钙与盐酸反应生成氯化钙和水,反应的化学方程式是:Ca(OH)2+2HCl═CaCl2+2H2O.
故填:Ca(OH)2+2HCl═CaCl2+2H2O.
(3)稀盐酸和氢氧化钠、氢氧化钙反应的化学方程式及其质量关系为:
NaOH+HCl═NaCl+H2O,Ca(OH)2+2HCl═CaCl2+2H2O,
40 36.5 74 73
由以上质量关系可知,中和相同质量的盐酸时,消耗的氢氧化钠质量大,因此 若用熟石灰中和相同质量的盐酸,所需的质量<ng.
故填:<.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:解答题
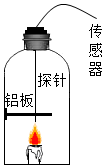 蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:
蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:| 相对湿度 | 氧气含量 | 二氧化碳含量 | 一氧化碳含量 | |
| 蜡烛点燃前 | 48.4% | 18.7% | 0.058% | 0 |
| 蜡烛熄灭后 | 71.6% | 15.6% | 3.643% | 0.018% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
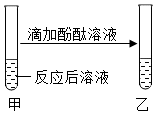 | 无色酚酞溶液变红色; | 溶液呈碱性,使其呈碱性的微粒是氢氧根离子; |
| 无色酚酞溶液不变色 | 溶液呈酸性或中性; |
| 实验操作 | 实验现象 | 实验结论 |
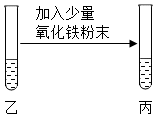 | 粉末部分或全部消失,溶液变为黄色 | 溶液呈酸性,反应的化学方程式是Fe2O3+6HCl═2FeCl3+3H2O; |
| 无明显变化 | 溶液呈中性; |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 构建知识网络是一种重要的学习方法.小科对物质组成和结构方面的知识进行了归纳,绘制了一张知识网络图.
构建知识网络是一种重要的学习方法.小科对物质组成和结构方面的知识进行了归纳,绘制了一张知识网络图.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 地球是一个水球,有90%的面积被水覆盖 | |
| B. | 陆地淡水几乎占地球总水量的$\frac{3}{4}$ | |
| C. | 冰融化为水后,体积变小 | |
| D. | 健康的成年人每天一般约摄水25升水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在空气中燃烧,产生大量白雾 | |
| B. | 硫在氧气中燃烧,发出蓝紫色火焰 | |
| C. | 木炭在空气中燃烧,生成黑色固体 | |
| D. | 铁丝在氧气中燃烧,生成四氧化三铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
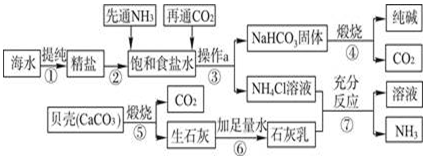
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com