
| 液体 | 甲 | 乙 | 丙 | 丁 |
| pH | 8.5 | 11.9 | 7.0 | 0.9 |
| A. | 甲 | B. | 乙 | C. | 丙 | D. | 丁 |
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:初中化学 来源: 题型:选择题
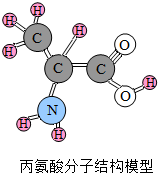 蛋白质是人类重要的营养物质,它是由多种氨基酸构成的化合物,丙氨酸就是其中的一种,下列关于丙氨酸的说法中正确的是( )
蛋白质是人类重要的营养物质,它是由多种氨基酸构成的化合物,丙氨酸就是其中的一种,下列关于丙氨酸的说法中正确的是( )| A. | 丙氨酸是由碳、氢、氧、氮四种原子构成的 | |
| B. | 丙氨酸分子中质子数是86 | |
| C. | 丙氨酸中氮元素和氢元素的质量比为2:1 | |
| D. | 丙氨酸的化学式是C3H6O2N |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子数比为1:1的CO和O2 | B. | 分子数比为1:2的CH4和O2 | ||
| C. | 质量比为3:6的C和O2 | D. | 质量比为1:8的H2和O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
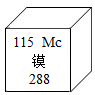 2017年5月,中国科学院,国家语言文字工作委员会,全国科学技术名词审定委员会在北京联合举行新闻发布会,正式向社会发布115号等元素的中文名称,115号元素的相关信息如图所示,有关该元素说法不正确的是( )
2017年5月,中国科学院,国家语言文字工作委员会,全国科学技术名词审定委员会在北京联合举行新闻发布会,正式向社会发布115号等元素的中文名称,115号元素的相关信息如图所示,有关该元素说法不正确的是( )| A. | 属于非金属元素 | B. | 原子序数为115 | C. | 元素名称为镆 | D. | 元素符号为Mc |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
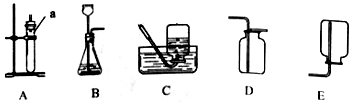
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
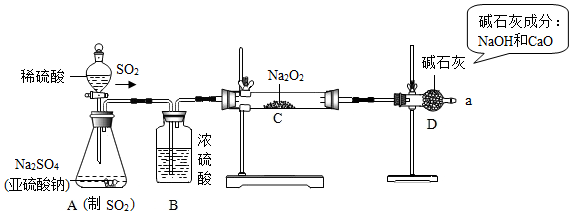
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com