
| (2)温度计能指示气温高低是利用了物质的热胀冷缩性质,就是由于物质分子间间隔受热时增大,遇冷时缩小形成的,故选B; (3)过氧化氢分解后产生了水和氧气,有新物质生成,所以分子发生了变化;故选D; (4)根据同种分子性质相同,不同种分子性质不同;碘和碘蒸气是同种分子的物质,都能燃烧;故选C.故答案为:(1)-A; (2)-B; (3)-D; (4)-C. 点评:本题考查学生对分子与原子的基本特征的理解与掌握,并能灵活用于解题的能力.
 
练习册系列答案
相关习题
科目:初中化学 来源: 题型: 4、将下列A组所叙述的现象和B组的解释要点用短线连接起来
查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解 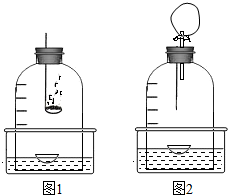 氮化镁“跑”到哪儿去了 氮化镁“跑”到哪儿去了小李老师发现,在空气中直接点燃镁条,根本观察不到镁与氮气反应的现象,产物中也检验不出氮化镁.生成的氮化镁究竟“跑”到哪儿去了?于是,他对该问题进行了探究. 1、仪器、药品 仪器:水槽、钟罩(内径15厘米、容积约为2300毫升)、 药品:镁条、蒸馏水、红色石蕊试纸 2、仪器装置 3、步骤、现象 (1)如图1所示,将一蒸发皿浮于水面,通过燃烧的红磷除去钟罩内的氧气,待充分冷却,观察到钟罩内的水面上升了原水面上方容积的1/5,得到了较为纯净的氮气. (2)往水槽内慢慢注水,使钟罩内外水面持平. (3)在一单孔塞上固定一家用保鲜薄膜袋,另一端插入一粗铜丝,铜丝下端悬挂一约25厘米长绕成螺旋状的光亮的镁条. (4)如图2所示,点燃镁条,同时拔出插有燃烧匙的塞子,立刻将燃烧着的镁条伸入钟罩内,并塞紧单孔塞.可观察到镁条与刚混入的少量氧气剧烈反应,冒出大量的白烟,发出耀眼的白光,放出的热使钟罩内的气体体积迅速膨胀,一会儿光的强度在减弱,变成了红光. (5)燃烧停止后,钟罩内的水面立刻上升,上端的内壁出现淡黄色粉未(氮化镁 (6)打开单孔塞,移走钟罩,把蒸发皿内的灰分转移至小试管内,加入1毫升蒸馏水,在试管口平放一湿润的红色石蕊试纸,加热到沸腾,可观察到红色石蕊试纸变蓝,反应方程式为:Mg3N2+6H2O?3Mg(OH)2↓+2NH3↑. 认真阅读以上材料,并回答以下问题: ①小李老师在装置中选用的是小气球还是家用保鲜袋?理由是什么? ②用什么词代替符号②,可以对氮化镁出现在钟罩内壁上端的现象作出解释? ③实验步骤(2)中,为什么要“往水槽内慢慢注水,使钟罩内外水面持平”? ④有人认为“Mg3N2在800℃时可分解成Mg和N2,Mg燃烧的火焰温度高于800℃,那么即使有Mg3N2生成,生成的Mg3N2也会分解,即燃烧的最终产物是MgO”;有人在理论上计算出“在500℃时,生成氧化镁与氮化镁的质量之比为108:1”.那么,请你谈谈“在空气中直接点燃镁条,根本观察不到镁与氮气反应的现象,产物中也检验不出氮化镁”的原因. 查看答案和解析>> 科目:初中化学 来源: 题型:解答题 把对应的现象和解释要点用直线连接起来 |