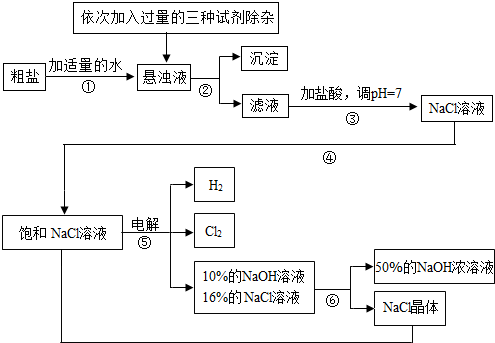
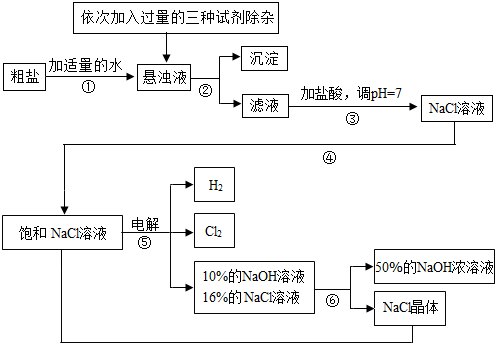
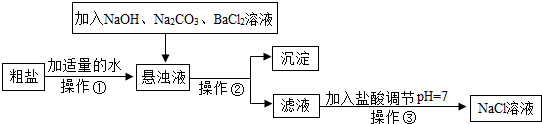
���ڴ����к�������MgCl
2��CaCl
2��Na
2SO
4�����ʣ������ϵ��Ҫ����˱��뾭�����ƣ��Դ���Ϊԭ�ϵġ��ȼҵ���������£�

�ش��������⣺
��1�������ڵ�������
����
����
�������ܵ�������
����
����
��
��2�������٢ڼ������ʱ���ӵ������Լ���NaOH��Һ��Na
2CO
3��Һ��BaCl
2��Һ��������������˳��Ҫ���ǣ�Na
2CO
3��Һ������BaCl
2��Һ֮
��
��
���ǰ�������룮
��ͬѧ�����
��������
��������
��Һ����BaCl
2��Һ�ɴﵽͬ����Ŀ�ģ�
��3����ȥ�Ȼ�þ�Ļ�ѧ����ʽ
2NaOH+MgCl2=Mg��OH��2��+2NaCl
2NaOH+MgCl2=Mg��OH��2��+2NaCl
��
��4����ⱥ��NaCl��Һ�Ļ�ѧ����ʽ��
2NaCl+2H
2O
2NaOH+H
2��+Cl
2��
2NaCl+2H
2O
2NaOH+H
2��+Cl
2��
��
��5���������п���ѭ�����õ�������
�Ȼ���
�Ȼ���
��




 ������������ϵ�д�
������������ϵ�д�