
【题目】化学从微观角度认识事物。
(1)根据下列粒子的结构示意图,回答问题。
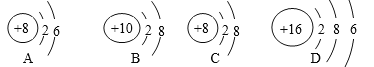
①属于同种元素的是___(填字母,下同)。
②具有相对稳定结构的原子是___。
③与A化学性质相似的是____。
(2)下图是甲和乙在一定条件下反应生成丙和丁的微观示意图,请根据图示回答问题。
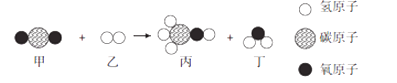
①一个丁分子是由_____构成的。
②该反应中甲和乙的分子数目比为___。
【答案】AC B D 两个氢原子和一个氧原子 1:3
【解析】
(1)①元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),同种元素的粒子是质子数相同,A、C的质子数相同,属于同种元素;
②B属于原子,且最外层为电子数均为8,属于相对稳定结构;
③元素性质与原子核外电子的排布,特别是最外层上的电子数目有密切关系,决定元素化学性质的是最外层电子数。A原子的最外层电子数为6,与B化学性质相似的微粒是D。
(2)反应的微观示意图可知,该反应是二氧化碳和氢气在一定条件下反应生成了甲醇和水,反应的方程式是:CO2+3H2 CH3OH+H2O 。
CH3OH+H2O 。
①由微粒的构成可知,一个丁分子是由两个氢原子和一个氧原子构成的;
②由上述方程式可知,该反应中甲和乙的分子数目比为1:3。


科目:初中化学 来源: 题型:
【题目】如图是实验室常用的两种气体制备、收集或净化的多种功能装置。
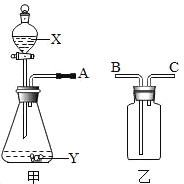
(1)若制备的气体是氧气,Y是黑色粉末,则甲中发生反应的化学方程式为_____。若用装满水的乙装置收集氧气,A端应与_____(填“B”或“C”)端相连。
(2)若制备的气体是CO2,则试剂X常用_____,Y是_____,用甲、乙两装置组成发生、净化CO2气体的装置。若乙装置中放入适量的浓硫酸,其作用是除去CO2气体中混有的_____;则A端应与_____(填“B”或“C”)端相连。
(3)若试剂Ⅹ是稀硫酸,Y是锌粒,则可以制取的气体是_____(填化学式);你认为能否用浓盐酸代替稀硫酸,理由是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )

A. 丁一定是该反应的催化剂
B. 该反应的基本类型是分解反应
C. 该反应中乙、丙的质量比为3:17
D. 该反应中甲、丙的质量比为7:4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色固体,可能含有碳酸钙、硫酸铜、氯化钠、硫酸钠、氯化钡中的一种或几种。为确定其组成,进行了如下实验。已知:氯化钡、硫酸钠溶液为中性。
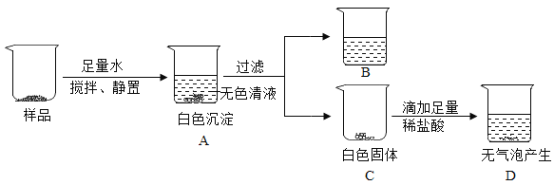
①白色固体中不含有CuSO4的依据是______。
②根据C、D现象,推出白色固体中一定没有______。
③烧杯B的溶液中一定含有______,理由是______(请用化学方程式表示)。
④设计实验探究B溶液中可能含有的成分,实验步骤如下:
Ⅰ.测溶液的pH
Ⅱ.取样,滴入足量Na2SO4溶液
Ⅲ.另取样,滴入足量Ba(NO3)2溶液
Ⅳ.待步骤Ⅲ充分反应后,取溶液于试管中,滴入AgNO3溶液
以上实验步骤没必要做的是______。
结论:这包白色固体一定有______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知 A、B、C、D、E 是初中化学常见的化合物,其中 B、C 都是氧化物, D 是一种碱,其相对分子质量为 74,A、B、D、E 属于不同类别的化合物。图中“—”表示相连的物质间能发生反应,“→”表示物质间存在转化关系。

(1)若A 属于盐,则E 属于_____,C 在生活中的一种用途是_____。
(2)若 A 属于酸,则 D 与E 反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是
![]()
A. C、CO2、CaCO3B. H2O2、H2O、O2
C. KOH、K2CO3、KNO3D. Fe2O3、FeCl3、Fe(OH)3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙点燃条件下反应生成丙和丁。反应前后分子变化的微观示意图如下:
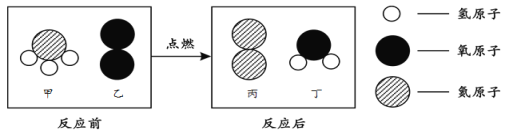
下列说法正确的是
A. 一个甲分子中含有2个原子B. 4种物质中,属于化合物的是甲和丁
C. 生成物丙和丁的质量比为28:18D. 该反应的基本类型为复分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
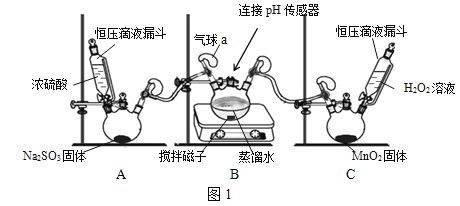
【题目】我国长江以南部分地区是世界三大酸雨区之一。某化学兴趣小组围绕酸雨的形成及燃煤电厂脱硫处理等问题进行探究。
I 模拟酸雨的形成
(查阅资料)
SO2转化为H2SO4的一条路径为:![]()
(操作步骤)
①组装仪器,检查装置气密性,装入药品。
②打开装置A中漏斗的活塞,启动装置B中的搅拌器,记录数据并绘图。
③待pH值稳定在3.73左右,打开装置C中漏斗的活塞。
④待pH值稳定在3.67左右,用注射器向气球a中注入H2O2溶液。
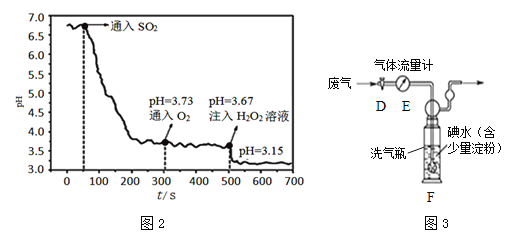
(问题讨论)
(1)装置A中发生的反应为Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O,其中Na2SO3中硫元素的化合价为______。装置C中发生反应的化学方程式为______。图1装置中安装气球的主要目的是______。
(2)向H2SO3中通入O2,H2SO3被氧化成酸性更强的H2SO4,但图2中pH变化不明显,这既与O2的氧化能力有关,又与氧气______的性质有关。注入H2O2溶液后,pH值明显降低,说明H2O2的氧化性比O2______(填“强”或“弱”)。
II 脱硫与SO2含量测定
(3)在燃煤中添加石灰石,SO2与石灰石、O2反应,生成硫酸钙和一种对环境无污染的气体,反应的化学方程式为______。下列措施能提高脱硫效率的是______。
A 无限延长脱硫时间 B 适当增加石灰石的用量
C 把工厂烟囱造得尽可能高 D 将石灰石和原煤粉碎并混合均匀
(4)已知燃煤电厂SO2排放标准为35mg/m3。小组同学设计图3装置进行实验:打开活塞D,将某燃煤电厂废气经气体流量计通入装置F(发生的反应为SO2+I2+2H2O===2HI+H2SO4),当碘水由蓝色褪为无色时,关闭活塞D,读出废气累计流量为3m3,若碘水中碘(I2)的质量为0.6g,计算该废气中SO2含量为______mg/m3(保留到小数点后一位),该厂废气______(填“符合”或“不符合”)排放标准。若装置F中蓝色消失后,没有及时关闭活塞D,测得的SO2含量将______(填“偏高”、“偏低”或“无影响”)。
III 知识拓展
自然界中的臭氧(O3)和H2O2能氧化H2SO3,大气污染物中含Fe、Cu、Mn、V的化合物能加快酸雨形成,一天内可在高空扩散700 多公里,所以酸雨不仅是区域性的危害,也是周边地区甚至跨国境的危害。
(5)由资料可知,大气中Fe、Cu、Mn、V的化合物可能充当了______的角色。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com