小凯与小组同学到实验室练习配制一定溶质质量分数的溶液.先称取纯净的氢氧化钠于洁净烧杯中,再量取自来水倒入烧杯中,搅拌后发现溶液中有白色浑浊物.对此现象小组同学都感到疑惑,于是进行了如下探究.
(实验室提供的试剂为:氢氧化钠固体、稀盐酸、蒸馏水、酚酞试液)
【提出问题】白色浑浊物是什么物质?
【查阅资料】①自来水是硬水,常常含有Ca(HCO3)2 和Mg(HCO3)2.
②Ca(HCO3)2 与足量的氢氧化钠反应方程式:Ca(HCO3)2+2NaOH=CaCO3↓+2H2O+Na2CO3,Mg(HCO3)2与足量的氢氧化钠反应方程式:Mg(HCO3)2+4NaOH=Mg(OH)2↓+2H2O+2Na2CO3
③Mg(OH)2在热水中溶解度增大,可形成稀溶液.
【作出猜想】
猜想一:白色浑浊物是CaCO3
猜想二:白色浑浊物是Mg(OH)2
猜想三:白色浑浊物是________.
【实验探究】
①取氢氧化钠于烧杯中,加自来水搅拌,杯壁发烫,原因是________.静置冷却、过滤.
②取①滤渣加稀盐酸,有气泡冒出,说明猜想________错误.
③若猜想三是正确的,在①和②的基础上,还应进行的操作是:________.
【拓展延伸】小凯认为实验探究①过滤后的滤液中溶质仅含有氢氧化钠,小组其他同学认为不正确.你的证明方法是:取滤液滴加足量的________,有气泡生成,说明滤液中还含有碳酸钠.则产生气泡的反应的化学方程式为:________.
【实验反思】
①实验室在配制溶液时应该使用________水.
②生活中降低水的硬度常用的方法是________.
CaCO3和Mg(OH)2 氢氧化钠溶于水放热 二 取①滤渣加热的蒸馏水,在上层清夜中再加酚酞试液 稀盐酸 Na2CO3+2HCl═2NaCl+H2O+CO2↑ 蒸馏 煮沸
分析:根据查阅资料:自来水是硬水,常常含有Ca(HCO3)2 和Mg(HCO3)2.Ca(HCO3)2+2NaOH=CaCO3↓+2H2O+Na2CO3,
Mg (HCO3)2+2NaOH=Mg(OH)2↓+2H2O+Na2CO3,及氢氧化钠溶解放出热量,而Mg(OH)2在热水中溶解度增大,可推测猜想三:白色浑浊物是白色浑浊物是CaCO3和Mg(OH)2;
根据猜想,滤液加稀盐酸,有气泡冒出,可推测滤液中还含有碳酸钠,可排除猜想二,由此写出反应的化学方程式;取①滤渣加热的蒸馏水,在上层清夜中再加酚酞试液,液体变红,可知含有OH-,由此可推断猜想三正确;
根据查阅资料,可推测实验探究①过滤后的滤液中含有碳酸钠,用鉴别碳酸钙的方法进行解答;由此可知实验室在配制溶液时应该使用蒸馏水(或纯水);用肥皂水可鉴别软硬水进行解答.
解答:根据查阅资料:自来水是硬水,常含有Ca(HCO3)2 和Mg(HCO3)2;Ca(HCO3)2+2NaOH=CaCO3↓+2H2O+Na2CO3,
Mg (HCO3)2+2NaOH=Mg(OH)2↓+2H2O+Na2CO3,及氢氧化钠溶解放出热量,而Mg(OH)2在热水中溶解度增大,可推测猜想三:白色浑浊物是白色浑浊物是CaCO3和Mg(OH)2;
【实验探究】
①取氢氧化钠于烧杯中,加自来水水搅拌,杯壁发烫,原因是:氢氧化钠溶解放出热量;故答案为:氢氧化钠溶解放出热量;
②取①滤渣加稀盐酸,有气泡冒出,说明猜想 二错误;
③若猜想三是正确的,在①和②的基础上,还应进行的操作是:取①滤渣加热的蒸馏水,在上层清夜中再加酚酞试液.
【拓展延伸】
根据猜想,滤渣加稀盐酸,有气泡冒出,可推测滤渣中含有含有碳酸钙,可排除猜想二,由此反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.故答案为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
【实验反思】
①通过上述实验可知实验室在配制溶液时应该使用蒸馏水(或纯水).故答案为:蒸馏水(或纯水);
②②生活中降低水的硬度常用的方法是 煮沸.故答案为:煮沸
点评:本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.



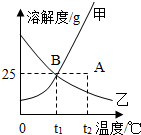 (1)如图为甲、乙两种固体物质在水中的溶解度曲线:
(1)如图为甲、乙两种固体物质在水中的溶解度曲线:
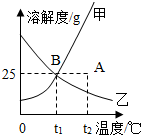 (1)如图为甲、乙两种固体物质在水中的溶解度曲线:
(1)如图为甲、乙两种固体物质在水中的溶解度曲线: