
| A. | 反应后的溶液可能为蓝色 | B. | 金属M可能是铝 | ||
| C. | M的金属活动性比Ag强 | D. | 反应前后M的化合价改变 |
分析 根据题意,金属M与AgNO3溶液反应的化学方程式为:M+2AgNO3═M(NO3)2+2Ag,可以看出:M的金属活动性比铜强;M(NO3)2中硝酸根显-1价,则M元素的化合价为+2价;据此进行分析判断.
解答 解:A、若反应后硝酸铜有剩余,则反应后的溶液可能为蓝色,故选项说法正确.
B、M(NO3)2中硝酸根显-1价,则M元素的化合价为+2价,而铝的化合价为+3价,则金属M不可能是铝,故选项说法错误.
C、金属M与AgNO3溶液反应的化学方程式为:M+2AgNO3═M(NO3)2+2Ag,可以看出:M的金属活动性比铜强,故选项说法正确.
D、反应物中M是单质,化合价为0;生成物M(NO3)2中,M元素显+2价;反应前后M的化合价改变,故选项说法正确.
故选:B.
点评 本题难度不大,熟练掌握金属的化学性质(前金换后金)、化合价的原则并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
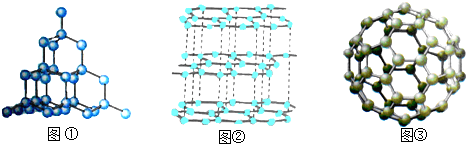
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| A | B |
| 火力发电厂常用石灰石浆吸收废气中的二氧化硫,以防止空气污染.反应的化学方程式为: 2CaCO3 +O2 +2SO2 ═2CaSO4 +2CO2 若处理含有1.6kg二氧化硫的废气,至少需要碳酸钙的质量为2.5kg才能将其完全吸收. | 原煤中含有硫,燃烧时生成的SO2会污染空气.测量SO2含量的化学方程式为: SO2+2H2O+I2═H2SO4+2HI,取用原煤燃烧产生的工业废气样品1m3,缓缓通过含碘(I2)1.27mg的碘溶液,刚好完全反应.则该工业废气中SO2的含量为0.32mg/m3(假设工业废气中的其它物质不与碘反应). |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 给试管中药品加热,需先预热 | |
| B. | 制取气体前,需先检查装置的气密性 | |
| C. | 连接乳胶管和玻璃导管,需先用水湿润 | |
| D. | 滴加少量液体时,需将胶头滴管伸入到容器中并紧贴容器内壁 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
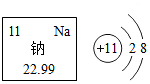 钠元素的相关信息如图,下列说法正确的是( )
钠元素的相关信息如图,下列说法正确的是( )| A. | 钠原子的中子数为11 | B. | 钠元素属于非金属元素 | ||
| C. | 钠原子核外有3个电子层 | D. | 钠原子的相对原子质量为22.99g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com