
ÓŠĮ½ĘæĘųĢ壬Ņ»ĘæŹĒ¶žŃõ»ÆĢ¼£»Ņ»ĘæŹĒŃõĘų£®ÄćÓĆŹ²Ć“·½·ØĒų±šĖüĆĒ£æ
 Š”ѧæĪŹ±ĢŲѵĻµĮŠ“š°ø
Š”ѧæĪŹ±ĢŲѵĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ²ĀĻė | ŹµŃé·½·Ø | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ | ||||
| øĆĘųĢåæÉÄÜ ŃõĘų ŃõĘų |
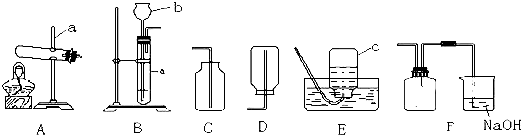
½« “ų»šŠĒµÄľĢõÉģČėŹŌ¹ÜÖŠ “ų»šŠĒµÄľĢõÉģČėŹŌ¹ÜÖŠ |
ľĢõø“Č¼ ľĢõø“Č¼ |
ŹµŃéŹŅÖĘČ”“ĖĘųĢå·“Ó¦µÄĪÄ×Ö±ķ“ļŹ½£ŗ ¹żŃõ»ÆĒā
¹żŃõ»ÆĒā
|
| ¼ÓČČ |
| ¼ÓČČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ŠņŗÅ | ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó |
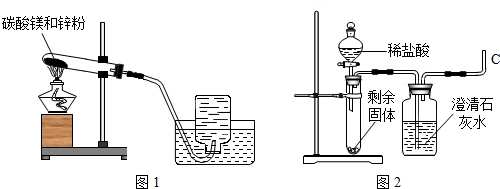
| ¢Ł | ŹÕ¼ÆĮ½ĘæĘųĢ壬øĒŗĆ²£Į§Ę¬£®ĻņĘäÖŠŅ»ĘæŃøĖŁµ¹ČėÉŁĮæ³ĪĒåŹÆ»ŅĖ®£¬øĒŗĆÕńµ“£® | ĪŽĆ÷ĻŌĻÖĻó£® |
| ¢Ś | ½«ĮķŅ»ĘæĘųĢåµćČ¼£¬“ż»šŃęĻØĆšŗó£¬ŃøĖŁµ¹ČėÉŁĮæ³ĪĒåŹÆ»ŅĖ®£¬øĒŗĆÕńµ“£® | ĘųĢå°²¾²Č¼ÉÕ£¬»šŃę³ŹĄ¶É«£¬³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£® |
| ||
| ||
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
æÕĘųÖŠµÄSO2ŗ¬ĮæŗĶæÉĪüČėæÅĮ£µÄŗ¬Įæ£ØæÉÓĆg/cm3±ķŹ¾£©¶¼ŹĒÖŲŅŖµÄæÕĘųÖŹĮæÖø±ź”£ŌŚ¹¤ŅµÉś²śÉĻ¹ę¶Ø£ŗæÕĘųÖŠ¶žŃõ»ÆĮņµÄ×ī“óŌŹŠķÅÅ·ÅÅØ¶Č²»µĆ³¬¹ż0.02 mg/L”£”¶2004Äź½ĖÕŹ”»·¾³×“æö¹«±Ø”·Öø³ö£ŗ½ĖÕŹ”2004Äź¹¤Ņµ(Ö÷ŅŖŹĒČȵē³§)¶žŃõ»ÆĮņÅÅ·Å×ÜĮæĪŖ1.24”Į106t£¬Č«Ź”ĖįÓźĪŪČ¾±Č½ĻŃĻÖŲ”£·ÖĪö½µÓź³É·Ö·¢ĻÖ£¬ÓźĖ®ÖŠŅõĄė×ÓČŌŅŌĮņĖįøłĄė×ÓĪŖÖ÷£¬Ō¼Õ¼ŅõĄė×Ó×ÜĮæµÄ61.9£„”£
£ØŅ»£©(1)Õż³£µÄÓźĖ®ĻŌ ŠŌ(Ģī:Ėį”¢¼ī”¢»ņÖŠ)£¬ŌŅņŹĒ £»
(2)ÓÉÓŚ“óĘųÖŠSO2ŗĶNOx(NOŗĶNO2)µÄŗ¬Įæ²»¶ĻÉżøߣ¬²¢×Ŗ±äĪŖH2SO4ŠĶŗĶHNO3ŠĶÓźĖ®½µĀä¶ųŠĪ³ÉµÄ”£ĪŅŹ”Ö÷ŅŖŹĒĮņĖįŠĶĖįÓź”£ĪŅŹ”ÕāÖÖĖįÓźŠĪ³É¹ż³ĢÓŠĮ½ÖÖĶ¾¾¶£ŗŅ»ÖÖŹĒSO2ŌŚæÕĘųÖŠµÄĘ®³¾×ö“߻ƼĮµÄ×÷ÓĆĻĀ±»ŃõĘųŃõ»ÆĪŖSO3£¬ČÜÓŚĖ®Éś³ÉĮņĖį£¬Š“³öÓŠ¹ŲµÄ·“Ó¦»Æѧ·½³ĢŹ½ ”¢ £»
ĮķŅ»ÖÖŹĒSO2ČÜÓŚĖ®Éś³ÉŃĒĮņĖį£¬ŌŁ±»æÕĘųÖŠµÄŃõĘųŃõ»Æ³ÉĮņĖį£¬Š“³öÓŠ¹ŲµÄ·“Ó¦»Æѧ·½³ĢŹ½ ”¢ ”£ÓÉÓŚSO2µÄŃõ»Æ·Ē³£»ŗĀż£¬¹ŹŗóŅ»ÖÖĶ¾¾¶ŹĒĘäÖ÷ŅŖŠĪ³É¹ż³Ģ”£
£Ø3£©ŠĖȤŠ”×éĶ¬Ń§Č”øÕ½µµ½Čȵē³§ø½½üµÄÓźĖ®½ųŠŠ²ā¶Ø£¬ĆæøōĪå·ÖÖÓ²āŅ»“ĪpH£¬Ę䏿¾ŻČēĻĀ±ķĖłŹ¾£ŗ
| ²ā¶ØŹ±æĢ | 5”Ć05 | 5”Ć10 | 5”Ć15 | 5”Ć20 | 5”Ć25 | 5”Ć30 | 5”Ć35 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |
·ÖĪöÉĻŹöŹż¾Ż±ä»Æ£¬ÄćæÉŅŌµĆ³öµÄ½įĀŪŹĒ £»Õė¶Ō“Ė½įĀŪ£¬Äć²Ā²āĘäÖŠµÄŌŅņĪŖ ”£½įŗĻ“óĄķŹÆ±»ĖįÓźøÆŹ“µÄŹĀŹµ£¬ÄćČĻĪŖĢ¼Ėį”¢ĮņĖį”¢ŃĒĮņĖįĖįŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖ__________________________”£
£Ø¶ž£©SO2ĘųĢåÄÜŹ¹Ę·ŗģČÜŅŗ”¢øßĆĢĖį¼ŲČÜŅŗĶŹÉ«”£

»Ų“šŅŌĻĀĪŹĢā£ŗ
£Ø1£©µ„¶Ą¼ģ²é×°ÖĆCµÄĘųĆÜŠŌµÄ²Ł×÷ŹĒ£ŗ¹Ų±Õ»īČūb£¬Č»ŗó________________________ £¬
Čō·¢ĻÖ________________£¬ĖµĆ÷×°ÖĆCĘųĆÜŠŌĮ¼ŗĆ”£
£Ø2£©ŹµŃéŹŅÓĆNa2SO3¹ĢĢåŗĶĮņĖįČÜŅŗÖĘČ”SO2ĘųĢå£¬Ó¦Ń”ÓĆ__________£ØŃ””°A”±»ņ”°C”±£©×öĘųĢå·¢Éś×°ÖĆ£¬²»Ń”ÓĆĮķŅ»×°ÖƵĥķÓÉŹĒ ”£
£Ø3£©Š”×éµÄĶ¬Ń§ŌŚA”¢C×°ÖĆÖŠµÄĮķŅ»øöÓĆæéדFeS¹ĢĢåŗĶĻ”ĮņĖįÖĘČ”H2SĘųĢ壬·“Ó¦µÄ·½³ĢŹ½ĪŖ_________________ ”£
£Ø4£©SO2ĘųĢåĶعżD×°ÖĆŹ±ĻÖĻóŹĒ____________________ £¬ĶعżE×°ÖĆŹ±ĻÖĻóŹĒ________________ £»SO2ÓėH2SŌŚB×°ÖĆÖŠ·“Ó¦£¬Éś³ÉŅ»ÖÖŃõ»ÆĪļŗĶŅ»ÖÖµ„ÖŹ£¬·“Ó¦µÄ·½³ĢŹ½ŹĒ ”£
£Ø5£©FŅĒĘ÷µÄĆū³ĘŹĒ___________£»FÖŠŹ¢ÓŠNaOH¹ĢĢ壬×÷ÓĆŹĒ
£ØČż£©¢ÅĪŖ²ā¶ØijµŲ·½µÄæÕĘųÖŠSO2ŗĶæÉĪüČėæÅĮ£µÄŗ¬Į棬²éŌÄ׏ĮĻµĆÖŖ£ŗæÉÓĆŗ¬ÓŠŅ»¶ØĮæµāµÄČÜŅŗ²ā¶ØæÕĘųÖŠµÄSO2ŗ¬Į棬·“Ó¦·½³ĢŹ½ŹĒ£ŗSO2£«I2£«2H2O£½H2SO4£«2HI”£¼×Ķ¬Ń§Éč¼ĘĮĖČēĻĀĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ£ŗ

¢ŁÓ¦ÓĆÉĻŹö×°ÖĆ²ā¶ØæÕĘųÖŠµÄSO2ŗ¬ĮæŗĶæÉĪüČėæÅĮ£µÄŗ¬Į棬³ż²ā¶ØĘųĢåĮ÷ĖŁ£Øµ„Ī»£ŗcm3/min£©Ķā£¬»¹ŠčŅŖ²ā¶ØĪüŹÕĒ°ŗóæÅĮ£Īüø½¼Į”¢ĆŽ»Ø”¢Ź¢·ÅČŻĘ÷µÄ×ÜÖŹĮæŗĶ ”£
¢ŚŅŃÖŖ£ŗµāµ„ÖŹĪ¢ČÜÓŚĖ®£¬KIæÉŅŌŌö“óµāŌŚĖ®ÖŠµÄČܽā¶Č”£
ĒėÄćŠÖś¼×Ķ¬Ń§Ķź³ÉĻ”µāČÜŅŗµÄÅäÖĘ£ŗ
µŚŅ»²½£ŗ×¼Č·³ĘČ”1.27gµāµ„ÖŹ¼ÓČėÉÕ±ÖŠ£¬ £»
µŚ¶ž²½£ŗ¼ÓŹŹĮæĖ®Ź¹Ö®ĶźČ«Čܽā£¬Č»ŗó¼ÓĖ®ÖĮČÜŅŗĢå»żĪŖ1000 mL£»
µŚČż²½£ŗ“ÓµŚ¶ž²½ĖłµĆČÜŅŗÖŠ£¬Č”³ö10.00mLČÜŅŗ¼ÓČėĻ”ŹĶÖĮ100mL”£
¢ĘŅŅĶ¬Ń§ÄāÓĆĻĀĮŠ¼ņŅ××°ÖĆ²ā¶ØæÕĘųÖŠµÄSO2ŗ¬Įæ£ŗ×¼Č·Č”50mLµŚČż²½ĖłµĆµÄµāČÜŅŗ£¬×¢ČėÓŅĶ¼ĖłŹ¾¹ćæŚĘæÖŠ£¬¼Ó2”«3µĪµķ·ŪÖøŹ¾¼Į£¬“ĖŹ±ČÜŅŗ³ŹĄ¶É«”£ŌŚÖø¶ØµÄ²ā¶ØµŲµć³éĘų£¬Ćæ“Ī³éĘų100mL£¬Ö±µ½ČÜŅŗµÄĄ¶É«Č«²æĶŹ¾”ĪŖÖ¹£¬¼ĒĀ¼³éĘų“ĪŹż£Øn£©”£
¼ŁÉčŅŅĶ¬Ń§µÄ²āĮæŹĒ×¼Č·µÄ£¬ŅŅĶ¬Ń§³éĘųµÄ“ĪŹżĪŖ80“Ī£¬¼ĘĖćĖµĆ÷øƵŲæÕĘųÖŠµÄSO2ŗ¬ĮæŹĒ·ń·ūŗĻÅŷűź×¼”££ØŠ“³ö½āĢā¹ż³Ģ£¬“ĖĢā3·Ö£©

¢ĒøĆŠ”×éĶ¬Ń§ČĻĪŖÕāŠ©¹¤³§ŅŖ¶ŌÅųöµÄ·ĻĘų½ųŠŠ“¦Ąķ£¬ĪŖĮĖ“ļµ½×īŗĆŠ§¹ū£¬ŌŚŹµŃéŹŅ½ųŠŠĮĖŹµŃéÄ£Äā£¬ÄćČĻĪŖĖūĆĒĪŖĮĖĪüŹÕ²śÉśµÄSO2ĘųĢ壬ĖłŹ¹ÓĆŅ©Ę·Ó¦øĆŹĒ________£¬·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½______________________________________
¾¹żŌŁČżĖ¼æ¼£¬Éč¼ĘĮĖŅŌĻĀ×°ÖĆ£¬ČĻĪŖĻĀĮŠÄÄÖÖ²»ÄܲÉÓĆ______,ŅņĪŖĘäĖū×°Öƶ¼¾ßÓŠ________×÷ÓĆ”£

A B C D E F G H I J
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2012½ģ¶ČŌĘÄĻŹ”³õČż×ŪŗĻø“Ļ°»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢ½¾æĢā
æÕĘųÖŠµÄSO2ŗ¬ĮæŗĶæÉĪüČėæÅĮ£µÄŗ¬Įæ£ØæÉÓĆg/cm3±ķŹ¾£©¶¼ŹĒÖŲŅŖµÄæÕĘųÖŹĮæÖø±ź”£ŌŚ¹¤ŅµÉś²śÉĻ¹ę¶Ø£ŗæÕĘųÖŠ¶žŃõ»ÆĮņµÄ×ī“óŌŹŠķÅÅ·ÅÅØ¶Č²»µĆ³¬¹ż0.02 mg/L”£”¶2004Äź½ĖÕŹ”»·¾³×“æö¹«±Ø”·Öø³ö£ŗ½ĖÕŹ”2004Äź¹¤Ņµ(Ö÷ŅŖŹĒČȵē³§)¶žŃõ»ÆĮņÅÅ·Å×ÜĮæĪŖ1.24”Į106t£¬Č«Ź”ĖįÓźĪŪČ¾±Č½ĻŃĻÖŲ”£·ÖĪö½µÓź³É·Ö·¢ĻÖ£¬ÓźĖ®ÖŠŅõĄė×ÓČŌŅŌĮņĖįøłĄė×ÓĪŖÖ÷£¬Ō¼Õ¼ŅõĄė×Ó×ÜĮæµÄ61.9£„”£
£ØŅ»£©(1)Õż³£µÄÓźĖ®ĻŌ ŠŌ(Ģī:Ėį”¢¼ī”¢»ņÖŠ)£¬ŌŅņŹĒ £»
(2)ÓÉÓŚ“óĘųÖŠSO2ŗĶNOx(NOŗĶNO2)µÄŗ¬Įæ²»¶ĻÉżøߣ¬²¢×Ŗ±äĪŖH2SO4ŠĶŗĶHNO3ŠĶÓźĖ®½µĀä¶ųŠĪ³ÉµÄ”£ĪŅŹ”Ö÷ŅŖŹĒĮņĖįŠĶĖįÓź”£ĪŅŹ”ÕāÖÖĖįÓźŠĪ³É¹ż³ĢÓŠĮ½ÖÖĶ¾¾¶£ŗŅ»ÖÖŹĒSO2ŌŚæÕĘųÖŠµÄĘ®³¾×ö“߻ƼĮµÄ×÷ÓĆĻĀ±»ŃõĘųŃõ»ÆĪŖSO3£¬ČÜÓŚĖ®Éś³ÉĮņĖį£¬Š“³öÓŠ¹ŲµÄ·“Ó¦»Æѧ·½³ĢŹ½ ”¢ £»
ĮķŅ»ÖÖŹĒSO2ČÜÓŚĖ®Éś³ÉŃĒĮņĖį£¬ŌŁ±»æÕĘųÖŠµÄŃõĘųŃõ»Æ³ÉĮņĖį£¬Š“³öÓŠ¹ŲµÄ·“Ó¦»Æѧ·½³ĢŹ½ ”¢ ”£ÓÉÓŚSO2µÄŃõ»Æ·Ē³£»ŗĀż£¬¹ŹŗóŅ»ÖÖĶ¾¾¶ŹĒĘäÖ÷ŅŖŠĪ³É¹ż³Ģ”£
£Ø3£©ŠĖȤŠ”×éĶ¬Ń§Č”øÕ½µµ½Čȵē³§ø½½üµÄÓźĖ®½ųŠŠ²ā¶Ø£¬ĆæøōĪå·ÖÖÓ²āŅ»“ĪpH£¬Ę䏿¾ŻČēĻĀ±ķĖłŹ¾£ŗ
|
²ā¶ØŹ±æĢ |
5”Ć05 |
5”Ć10 |
5”Ć15 |
5”Ć20 |
5”Ć25 |
5”Ć30 |
5”Ć35 |
|
pH |
4.95 |
4.94 |
4.94 |
4.88 |
4.86 |
4.85 |
4.85 |
·ÖĪöÉĻŹöŹż¾Ż±ä»Æ£¬ÄćæÉŅŌµĆ³öµÄ½įĀŪŹĒ £»Õė¶Ō“Ė½įĀŪ£¬Äć²Ā²āĘäÖŠµÄŌŅņĪŖ ”£½įŗĻ“óĄķŹÆ±»ĖįÓźøÆŹ“µÄŹĀŹµ£¬ÄćČĻĪŖĢ¼Ėį”¢ĮņĖį”¢ŃĒĮņĖįĖįŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖ__________________________”£
£Ø¶ž£©SO2 ĘųĢåÄÜŹ¹Ę·ŗģČÜŅŗ”¢øßĆĢĖį¼ŲČÜŅŗĶŹÉ«”£

»Ų“šŅŌĻĀĪŹĢā£ŗ
£Ø1£©µ„¶Ą¼ģ²é×°ÖĆCµÄĘųĆÜŠŌµÄ²Ł×÷ŹĒ£ŗ¹Ų±Õ»īČūb£¬Č»ŗó________________________ £¬
Čō·¢ĻÖ________________£¬ĖµĆ÷×°ÖĆCĘųĆÜŠŌĮ¼ŗĆ”£
£Ø2£©ŹµŃéŹŅÓĆNa2SO3¹ĢĢåŗĶĮņĖįČÜŅŗÖĘČ”SO2ĘųĢå£¬Ó¦Ń”ÓĆ__________£ØŃ””°A”±»ņ”°C”±£©×öĘųĢå·¢Éś×°ÖĆ£¬²»Ń”ÓĆĮķŅ»×°ÖƵĥķÓÉŹĒ ”£
£Ø3£©Š”×éµÄĶ¬Ń§ŌŚA”¢C×°ÖĆÖŠµÄĮķŅ»øöÓĆæéדFeS¹ĢĢåŗĶĻ”ĮņĖįÖĘČ”H2SĘųĢ壬·“Ó¦µÄ·½³ĢŹ½ĪŖ_________________ ”£
£Ø4£©SO2ĘųĢåĶعżD×°ÖĆŹ±ĻÖĻóŹĒ____________________ £¬ĶعżE×°ÖĆŹ±ĻÖĻóŹĒ________________ £»SO2ÓėH2SŌŚB×°ÖĆÖŠ·“Ó¦£¬Éś³ÉŅ»ÖÖŃõ»ÆĪļŗĶŅ»ÖÖµ„ÖŹ£¬·“Ó¦µÄ·½³ĢŹ½ŹĒ ”£
£Ø5£©FŅĒĘ÷µÄĆū³ĘŹĒ___________£»FÖŠŹ¢ÓŠNaOH¹ĢĢ壬×÷ÓĆŹĒ
£ØČż£©¢ÅĪŖ²ā¶ØijµŲ·½µÄæÕĘųÖŠSO2ŗĶæÉĪüČėæÅĮ£µÄŗ¬Į棬²éŌÄ׏ĮĻµĆÖŖ£ŗæÉÓĆŗ¬ÓŠŅ»¶ØĮæµāµÄČÜŅŗ²ā¶ØæÕĘųÖŠµÄSO2ŗ¬Į棬·“Ó¦·½³ĢŹ½ŹĒ£ŗSO2£«I2£«2H2O£½H2SO4£«2HI”£¼×Ķ¬Ń§Éč¼ĘĮĖČēĻĀĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ£ŗ
¢ŁÓ¦ÓĆÉĻŹö×°ÖĆ²ā¶ØæÕĘųÖŠµÄSO2ŗ¬ĮæŗĶæÉĪüČėæÅĮ£µÄŗ¬Į棬³ż²ā¶ØĘųĢåĮ÷ĖŁ£Øµ„Ī»£ŗcm3/min£©Ķā£¬»¹ŠčŅŖ²ā¶ØĪüŹÕĒ°ŗóæÅĮ£Īüø½¼Į”¢ĆŽ»Ø”¢Ź¢·ÅČŻĘ÷µÄ×ÜÖŹĮæŗĶ ”£
¢ŚŅŃÖŖ£ŗµāµ„ÖŹĪ¢ČÜÓŚĖ®£¬KIæÉŅŌŌö“óµāŌŚĖ®ÖŠµÄČܽā¶Č”£
ĒėÄćŠÖś¼×Ķ¬Ń§Ķź³ÉĻ”µāČÜŅŗµÄÅäÖĘ£ŗ
µŚŅ»²½£ŗ×¼Č·³ĘČ”1.27gµāµ„ÖŹ¼ÓČėÉÕ±ÖŠ£¬ £»
µŚ¶ž²½£ŗ¼ÓŹŹĮæĖ®Ź¹Ö®ĶźČ«Čܽā£¬Č»ŗó¼ÓĖ®ÖĮČÜŅŗĢå»żĪŖ1000 mL£»
µŚČż²½£ŗ“ÓµŚ¶ž²½ĖłµĆČÜŅŗÖŠ£¬Č”³ö10.00mLČÜŅŗ¼ÓČėĻ”ŹĶÖĮ100 mL”£
¢ĘŅŅĶ¬Ń§ÄāÓĆĻĀĮŠ¼ņŅ××°ÖĆ²ā¶ØæÕĘųÖŠµÄSO2ŗ¬Įæ£ŗ×¼Č·Č”50mLµŚČż²½ĖłµĆµÄµāČÜŅŗ£¬×¢ČėÓŅĶ¼ĖłŹ¾¹ćæŚĘæÖŠ£¬¼Ó2”«3µĪµķ·ŪÖøŹ¾¼Į£¬“ĖŹ±ČÜŅŗ³ŹĄ¶É«”£ŌŚÖø¶ØµÄ²ā¶ØµŲµć³éĘų£¬Ćæ“Ī³éĘų100mL£¬Ö±µ½ČÜŅŗµÄĄ¶É«Č«²æĶŹ¾”ĪŖÖ¹£¬¼ĒĀ¼³éĘų“ĪŹż£Øn£©”£
¼ŁÉčŅŅĶ¬Ń§µÄ²āĮæŹĒ×¼Č·µÄ£¬ŅŅĶ¬Ń§³éĘųµÄ“ĪŹżĪŖ80“Ī£¬¼ĘĖćĖµĆ÷øƵŲæÕĘųÖŠµÄSO2ŗ¬ĮæŹĒ·ń·ūŗĻÅŷűź×¼”££ØŠ“³ö½āĢā¹ż³Ģ£¬“ĖĢā3·Ö£©

¢ĒøĆŠ”×éĶ¬Ń§ČĻĪŖÕāŠ©¹¤³§ŅŖ¶ŌÅųöµÄ·ĻĘų½ųŠŠ“¦Ąķ£¬ĪŖĮĖ“ļµ½×īŗĆŠ§¹ū£¬ŌŚŹµŃéŹŅ½ųŠŠĮĖŹµŃéÄ£Äā£¬ÄćČĻĪŖĖūĆĒĪŖĮĖĪüŹÕ²śÉśµÄSO2 ĘųĢ壬ĖłŹ¹ÓĆŅ©Ę·Ó¦øĆŹĒ________£¬·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½______________________________________
¾¹żŌŁČżĖ¼æ¼£¬Éč¼ĘĮĖŅŌĻĀ×°ÖĆ£¬ČĻĪŖĻĀĮŠÄÄÖÖ²»ÄܲÉÓĆ______,ŅņĪŖĘäĖū×°Öƶ¼¾ßÓŠ________×÷ÓĆ”£

A B C D E F G H I J
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğŌĘÄĻŹ”ĆÉ×ŌŹŠ²©ĶØ×ÜŠ£³õČż»Æѧ×ŪŗĻø“Ļ°»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢ½¾æĢā
æÕĘųÖŠµÄSO2ŗ¬ĮæŗĶæÉĪüČėæÅĮ£µÄŗ¬Įæ£ØæÉÓĆg/cm3±ķŹ¾£©¶¼ŹĒÖŲŅŖµÄæÕĘųÖŹĮæÖø±ź”£ŌŚ¹¤ŅµÉś²śÉĻ¹ę¶Ø£ŗæÕĘųÖŠ¶žŃõ»ÆĮņµÄ×ī“óŌŹŠķÅÅ·ÅÅØ¶Č²»µĆ³¬¹ż0.02 mg/L”£”¶2004Äź½ĖÕŹ”»·¾³×“æö¹«±Ø”·Öø³ö£ŗ½ĖÕŹ”2004Äź¹¤Ņµ(Ö÷ŅŖŹĒČȵē³§)¶žŃõ»ÆĮņÅÅ·Å×ÜĮæĪŖ1.24”Į106t£¬Č«Ź”ĖįÓźĪŪČ¾±Č½ĻŃĻÖŲ”£·ÖĪö½µÓź³É·Ö·¢ĻÖ£¬ÓźĖ®ÖŠŅõĄė×ÓČŌŅŌĮņĖįøłĄė×ÓĪŖÖ÷£¬Ō¼Õ¼ŅõĄė×Ó×ÜĮæµÄ61.9£„”£
£ØŅ»£©(1)Õż³£µÄÓźĖ®ĻŌ ŠŌ(Ģī:Ėį”¢¼ī”¢»ņÖŠ)£¬ŌŅņŹĒ £»
(2)ÓÉÓŚ“óĘųÖŠSO2ŗĶNOx(NOŗĶNO2)µÄŗ¬Įæ²»¶ĻÉżøߣ¬²¢×Ŗ±äĪŖH2SO4ŠĶŗĶHNO3ŠĶÓźĖ®½µĀä¶ųŠĪ³ÉµÄ”£ĪŅŹ”Ö÷ŅŖŹĒĮņĖįŠĶĖįÓź”£ĪŅŹ”ÕāÖÖĖįÓźŠĪ³É¹ż³ĢÓŠĮ½ÖÖĶ¾¾¶£ŗŅ»ÖÖŹĒSO2ŌŚæÕĘųÖŠµÄĘ®³¾×ö“߻ƼĮµÄ×÷ÓĆĻĀ±»ŃõĘųŃõ»ÆĪŖSO3£¬ČÜÓŚĖ®Éś³ÉĮņĖį£¬Š“³öÓŠ¹ŲµÄ·“Ó¦»Æѧ·½³ĢŹ½ ”¢ £»
ĮķŅ»ÖÖŹĒSO2ČÜÓŚĖ®Éś³ÉŃĒĮņĖį£¬ŌŁ±»æÕĘųÖŠµÄŃõĘųŃõ»Æ³ÉĮņĖį£¬Š“³öÓŠ¹ŲµÄ·“Ó¦»Æѧ·½³ĢŹ½ ”¢ ”£ÓÉÓŚSO2µÄŃõ»Æ·Ē³£»ŗĀż£¬¹ŹŗóŅ»ÖÖĶ¾¾¶ŹĒĘäÖ÷ŅŖŠĪ³É¹ż³Ģ”£
£Ø3£©ŠĖȤŠ”×éĶ¬Ń§Č”øÕ½µµ½Čȵē³§ø½½üµÄÓźĖ®½ųŠŠ²ā¶Ø£¬ĆæøōĪå·ÖÖÓ²āŅ»“ĪpH£¬Ę䏿¾ŻČēĻĀ±ķĖłŹ¾£ŗ
|
²ā¶ØŹ±æĢ |
5”Ć05 |
5”Ć10 |
5”Ć15 |
5”Ć20 |
5”Ć25 |
5”Ć30 |
5”Ć35 |
|
pH |
4.95 |
4.94 |
4.94 |
4.88 |
4.86 |
4.85 |
4.85 |
·ÖĪöÉĻŹöŹż¾Ż±ä»Æ£¬ÄćæÉŅŌµĆ³öµÄ½įĀŪŹĒ £»Õė¶Ō“Ė½įĀŪ£¬Äć²Ā²āĘäÖŠµÄŌŅņĪŖ ”£½įŗĻ“óĄķŹÆ±»ĖįÓźøÆŹ“µÄŹĀŹµ£¬ÄćČĻĪŖĢ¼Ėį”¢ĮņĖį”¢ŃĒĮņĖįĖįŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖ__________________________”£
£Ø¶ž£©SO2 ĘųĢåÄÜŹ¹Ę·ŗģČÜŅŗ”¢øßĆĢĖį¼ŲČÜŅŗĶŹÉ«”£

»Ų“šŅŌĻĀĪŹĢā£ŗ
£Ø1£©µ„¶Ą¼ģ²é×°ÖĆCµÄĘųĆÜŠŌµÄ²Ł×÷ŹĒ£ŗ¹Ų±Õ»īČūb£¬Č»ŗó________________________ £¬
Čō·¢ĻÖ________________£¬ĖµĆ÷×°ÖĆCĘųĆÜŠŌĮ¼ŗĆ”£
£Ø2£©ŹµŃéŹŅÓĆNa2SO3¹ĢĢåŗĶĮņĖįČÜŅŗÖĘČ”SO2ĘųĢå£¬Ó¦Ń”ÓĆ__________£ØŃ””°A”±»ņ”°C”±£©×öĘųĢå·¢Éś×°ÖĆ£¬²»Ń”ÓĆĮķŅ»×°ÖƵĥķÓÉŹĒ ”£
£Ø3£©Š”×éµÄĶ¬Ń§ŌŚA”¢C×°ÖĆÖŠµÄĮķŅ»øöÓĆæéדFeS¹ĢĢåŗĶĻ”ĮņĖįÖĘČ”H2SĘųĢ壬·“Ó¦µÄ·½³ĢŹ½ĪŖ_________________ ”£
£Ø4£©SO2ĘųĢåĶعżD×°ÖĆŹ±ĻÖĻóŹĒ____________________ £¬ĶعżE×°ÖĆŹ±ĻÖĻóŹĒ________________ £»SO2ÓėH2SŌŚB×°ÖĆÖŠ·“Ó¦£¬Éś³ÉŅ»ÖÖŃõ»ÆĪļŗĶŅ»ÖÖµ„ÖŹ£¬·“Ó¦µÄ·½³ĢŹ½ŹĒ ”£
£Ø5£©FŅĒĘ÷µÄĆū³ĘŹĒ___________£»FÖŠŹ¢ÓŠNaOH¹ĢĢ壬×÷ÓĆŹĒ
£ØČż£©¢ÅĪŖ²ā¶ØijµŲ·½µÄæÕĘųÖŠSO2ŗĶæÉĪüČėæÅĮ£µÄŗ¬Į棬²éŌÄ׏ĮĻµĆÖŖ£ŗæÉÓĆŗ¬ÓŠŅ»¶ØĮæµāµÄČÜŅŗ²ā¶ØæÕĘųÖŠµÄSO2ŗ¬Į棬·“Ó¦·½³ĢŹ½ŹĒ£ŗSO2£«I2£«2H2O£½H2SO4£«2HI”£¼×Ķ¬Ń§Éč¼ĘĮĖČēĻĀĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ£ŗ
¢ŁÓ¦ÓĆÉĻŹö×°ÖĆ²ā¶ØæÕĘųÖŠµÄSO2ŗ¬ĮæŗĶæÉĪüČėæÅĮ£µÄŗ¬Į棬³ż²ā¶ØĘųĢåĮ÷ĖŁ£Øµ„Ī»£ŗcm3/min£©Ķā£¬»¹ŠčŅŖ²ā¶ØĪüŹÕĒ°ŗóæÅĮ£Īüø½¼Į”¢ĆŽ»Ø”¢Ź¢·ÅČŻĘ÷µÄ×ÜÖŹĮæŗĶ ”£
¢ŚŅŃÖŖ£ŗµāµ„ÖŹĪ¢ČÜÓŚĖ®£¬KIæÉŅŌŌö“óµāŌŚĖ®ÖŠµÄČܽā¶Č”£
ĒėÄćŠÖś¼×Ķ¬Ń§Ķź³ÉĻ”µāČÜŅŗµÄÅäÖĘ£ŗ
µŚŅ»²½£ŗ×¼Č·³ĘČ”1.27gµāµ„ÖŹ¼ÓČėÉÕ±ÖŠ£¬ £»
µŚ¶ž²½£ŗ¼ÓŹŹĮæĖ®Ź¹Ö®ĶźČ«Čܽā£¬Č»ŗó¼ÓĖ®ÖĮČÜŅŗĢå»żĪŖ1000 mL£»
µŚČż²½£ŗ“ÓµŚ¶ž²½ĖłµĆČÜŅŗÖŠ£¬Č”³ö10.00mLČÜŅŗ¼ÓČėĻ”ŹĶÖĮ100 mL”£
¢ĘŅŅĶ¬Ń§ÄāÓĆĻĀĮŠ¼ņŅ××°ÖĆ²ā¶ØæÕĘųÖŠµÄSO2ŗ¬Įæ£ŗ×¼Č·Č”50mLµŚČż²½ĖłµĆµÄµāČÜŅŗ£¬×¢ČėÓŅĶ¼ĖłŹ¾¹ćæŚĘæÖŠ£¬¼Ó2”«3µĪµķ·ŪÖøŹ¾¼Į£¬“ĖŹ±ČÜŅŗ³ŹĄ¶É«”£ŌŚÖø¶ØµÄ²ā¶ØµŲµć³éĘų£¬Ćæ“Ī³éĘų100mL£¬Ö±µ½ČÜŅŗµÄĄ¶É«Č«²æĶŹ¾”ĪŖÖ¹£¬¼ĒĀ¼³éĘų“ĪŹż£Øn£©”£
¼ŁÉčŅŅĶ¬Ń§µÄ²āĮæŹĒ×¼Č·µÄ£¬ŅŅĶ¬Ń§³éĘųµÄ“ĪŹżĪŖ80“Ī£¬¼ĘĖćĖµĆ÷øƵŲæÕĘųÖŠµÄSO2ŗ¬ĮæŹĒ·ń·ūŗĻÅŷűź×¼”££ØŠ“³ö½āĢā¹ż³Ģ£¬“ĖĢā3·Ö£©

¢ĒøĆŠ”×éĶ¬Ń§ČĻĪŖÕāŠ©¹¤³§ŅŖ¶ŌÅųöµÄ·ĻĘų½ųŠŠ“¦Ąķ£¬ĪŖĮĖ“ļµ½×īŗĆŠ§¹ū£¬ŌŚŹµŃéŹŅ½ųŠŠĮĖŹµŃéÄ£Äā£¬ÄćČĻĪŖĖūĆĒĪŖĮĖĪüŹÕ²śÉśµÄSO2 ĘųĢ壬ĖłŹ¹ÓĆŅ©Ę·Ó¦øĆŹĒ________£¬·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½______________________________________
¾¹żŌŁČżĖ¼æ¼£¬Éč¼ĘĮĖŅŌĻĀ×°ÖĆ£¬ČĻĪŖĻĀĮŠÄÄÖÖ²»ÄܲÉÓĆ______,ŅņĪŖĘäĖū×°Öƶ¼¾ßÓŠ________×÷ÓĆ”£

A B C D E F G H I J
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com