


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:初中化学 来源:化学教研室 题型:013
某铁的样品
5.6g投入足量的稀硫酸中,反应完全后生成0.21g的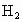 .则样品的成分可能是
.则样品的成分可能是
[
]|
A .生铁 |
B .纯铁 |
|
C .铁锌合金 |
D .生铁与镁的混合物 |
查看答案和解析>>
科目:初中化学 来源:中考必读·名校备考方案·化学 题型:038
锌粉、铝粉、铁粉、镁粉的混合物5 g与一定溶质质量分数为25%的稀硫酸恰好完全反应,将反应后的混合物蒸发水分得固体(不含结晶水)9.8 g,则反应中生成氢气的质量为多少?
查看答案和解析>>
科目:初中化学 来源: 题型:013
某铁的样品
5.6g投入足量的稀硫酸中,反应完全后生成0.21g的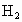 .则样品的成分可能是
.则样品的成分可能是
[
]|
A .生铁 |
B .纯铁 |
|
C .铁锌合金 |
D .生铁与镁的混合物 |
查看答案和解析>>
科目:初中化学 来源:2012-2013学年江苏省南京市白下区九年级(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com