
分析 (1)由题意可知赤铁矿石中的杂质既不容易酸,也不溶于水,而且该题目中涉及的化学反应也不会生成沉淀,所以滤渣的质量就是赤铁矿石中杂质的质量.那么样品中Fe2O3的质量=用样品的质量-杂质的质量.
(2)由氧化铁的质量根据氧化铁与稀盐酸反应的化学方程式可以计算出稀盐酸中溶质的质量分数.
解答 解:(1)依据题意可知,赤铁矿中氧化铁的质量为:20.0g-4.0g=16.0g;
赤铁矿石样品中的Fe2O3的质量分数为 $\frac{16g}{20g}$×100%=80.0%;
(2)设消耗氯化氢的质量是x;
Fe2O3+6HCl═2FeCl3+3 H2O
160 219
16g x
$\frac{160}{16g}=\frac{219}{x}$
x=21.9g
稀盐酸的溶质质量分数$\frac{21.9g}{184g}$×100%=11.9%
答:(1)赤铁矿石样品中Fe2O3的质量为16.0g,其纯度为80.0%;
(2)稀盐酸的溶质质量分数11.9%.
点评 这是一道常见的化学综合计算题.解题的关键在于弄清化学反应中反应物、生成物之间的关系,同时要弄清杂质在反应中存在于什么地方.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
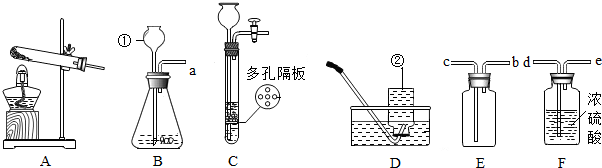
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 乙醇汽油中添加的乙醇属于可再生能源 | |
| B. | 氢气作为能源具有来源广、热值高、无污染等优点,目前氢能已得到大规模的应用 | |
| C. | 将煤球制成“蜂窝煤”是为了增大与空气的接触面积,使其燃烧更充分 | |
| D. | 我国南海海底储藏了大量“可燃冰”,它将成为未来重要的能源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com