
分析 (1)从生理盐水中有氯化钠和水去分析解答;
(2)从配制500g生理盐水的步骤及每一步需要的仪器去分析解答;
(3)从饱和溶液和不饱和溶液中溶质与溶剂的关系去分析解答.
解答 解:(1)生理盐水中有氯化钠和水,其中氯化钠是固体,水是液体,所以氯化钠是溶质;
故答案为:NaCl
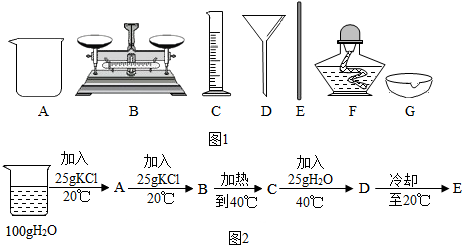
(2)配制500g生理盐水,需要用托盘天平称量500g×0.9%=4.5g的食盐,和用量筒量取495.5ml的水,并把食盐和水放在烧杯里溶解,并作玻璃棒进行搅拌;故答案为:ABCE;
(3)已知KCl的溶解度20℃时为34g.其含义为:在20℃时在100g水里,最多能溶解34g氯化钾;
在A中,由于氯化钾的质量25g<34g,此时所得溶液为不饱和溶液,溶质的质量分数为:$\frac{25g}{25g+100g}$×100%=20%;
在B中,溶质质量为25g+25g=50g,但在20℃在100g水里,最多能溶解34g氯化钾,此时溶质有剩余:50g-34g=16g,因此溶液中的溶质与溶剂的质量比为:34g:100g=17:50;溶质的质量分数为:$\frac{34g}{34g+100g}$×100%=25.4%;
在C中在40℃时,此时由于氯化钾的溶解度为40g,C中的溶质仍有剩余(50g-40g=10g);溶质的质量分数为:$\frac{40g}{40g+100g}$×100%=28.6%;
在D中设125g水中最多溶解氯化钾的质量为X,
40g/100g=X/125g;解之得:X=50g;故此时溶液恰好饱和;
溶质的质量分数为:$\frac{50g}{50g+125g}$×100%=28.6%
在E中当冷却到20℃时,100g水中最多可溶解34氯化钾,由于溶液具有均一性,所以125g水中最多可溶解42.5g,此时为饱和溶液,故溶质的质量分数为:$\frac{42.5g}{42.5g+125g}$×100%=25.4%;
由上面的分析可知答案为:B与E和C与D.
点评 计算溶质质量分数时剩余的溶质不能参与计算.


科目:初中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
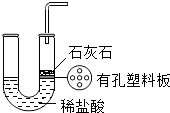 实验室用石灰石与稀盐酸反应制取二氧化碳,发生装置如图所示,从U形管注入稀盐酸,发现稀盐酸未能与有孔塑料板上的石灰石接触,但此时已无稀盐酸可加,则下列溶液中,最适宜添加的是( )
实验室用石灰石与稀盐酸反应制取二氧化碳,发生装置如图所示,从U形管注入稀盐酸,发现稀盐酸未能与有孔塑料板上的石灰石接触,但此时已无稀盐酸可加,则下列溶液中,最适宜添加的是( )| A. | 氢氧化钠溶液 | B. | 碳酸钠溶液 | C. | 氯化钠溶液 | D. | 澄清石灰水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 加入盐酸的质量g | 0 | 25 | 37.5 |
| 锥形瓶中物质的质量g | 45 | 70 | 80.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com