
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
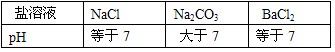
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
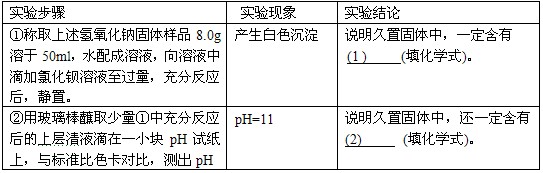
| ①称取上述氢氧化钠固体样品8.0g溶于50mL水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块儿pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品8.0g溶于50mL水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有 Na2C03 Na2C03 (填化学式). |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH 试纸上,与标准比色卡对比,测出pH. | pH=11 | 说明久置固体中,还一定含有 NaOH NaOH (填化学式). |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
(10株洲30).(7分)化学老师谢××交给某研究性学习小组一个任务:测定实验室里一瓶久置的NaOH固体是否变质。该小组的同学进行了如下实验探究:
【提出问题】 猜想I:没变质,全部是NaOH;猜想II:部分变质,既含有NaOH{又
含有Na2CO3:猜想Ⅲ:完全变质,全部是Na2CO3。
【查阅资料】①已知反应:BaCl2+Na2CO3=2NaCl+BaCO3↓
②部分盐溶液在常温下的pH如下:
| 盐溶液 | NaCI | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
【设计方案并进行实验】请你与他们一起共同完成,并回答所给问题。
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品8.0g溶于50ml,水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置。 | 产生白色沉淀 | 说明久置固体中,一定含有 (1 ) (填化学式)。 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有 (2) (填化学式)。 |
上述步骤①中,所用称量仪器的名称是 (3) ,滴加过量BaCl2溶液的目的是 (4)
【实验结论】通过实验,说明上述猜想中 (5) 是正确的。
【拓展】该小组同学为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、
干燥,称得其质量为2.0g,则原试剂中NaOH的质量分数为 (6) (假定试剂中无其它杂质)。
【反思】久置的氢氧化钠变质的原因是 (7) (用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
| 盐溶液 | NaCI | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品8.0g溶于50ml,水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置。 | 产生白色沉淀 | 说明久置固体中,一定含有 (1 ) (填化学式)。 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有 (2) (填化学式)。 |
查看答案和解析>>
科目:初中化学 来源:株洲 题型:问答题
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品8.0g溶于50mL水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有______(填化学式). |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块儿pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有______(填化学式). |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com