
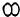 ���͡�
���͡� ���ֱ�������ֲ�ͬ�ĵ��ʷ���A2��B2��������һ���������ܷ�����ѧ��Ӧ���䷴Ӧ����ʾ��ͼ���£�
���ֱ�������ֲ�ͬ�ĵ��ʷ���A2��B2��������һ���������ܷ�����ѧ��Ӧ���䷴Ӧ����ʾ��ͼ���£�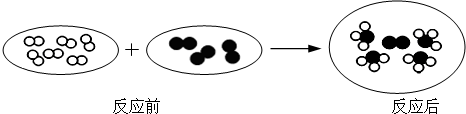
 �������ԭ�������ǡ�
�������ԭ�������ǡ� ����14������μӷ�Ӧ��A2�������������֮��Ϊ3��17��
����14������μӷ�Ӧ��A2�������������֮��Ϊ3��17�� ���� ��1�����ݷ�Ӧ�������֣���������һ�ַ�����
��2������������������ӵ�ģ�ͷ�����
��3�����ݷ�Ӧǰ��ԭ�ӵ����ࡢ��Ŀ��������ǵķ��ӹ��ɷ�����
��4������������ķ��ӽṹ������ɣ�
��5�����ݸ÷�Ӧ��A2��������ķ��Ӹ����ȷ������
��� �⣺���ڷ�Ӧǰ�������ͬ�ķ��ӣ����Ը�ͼʾ����ת��Ϊ��ͼ�������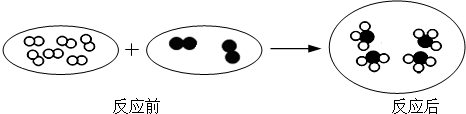
��1����ͼʾ��֪�÷�Ӧ��Ӧ�������֣���������һ�֣����������Ϸ�Ӧ��
��2������������ӵ�ģ�Ϳɿ������������ʵķ��������ֲ�ͬ��ԭ�ӹ��ɣ����Ը�����Ϊ�����
��3����ͼʾ��֪�÷�Ӧ��B2����������ӵĸ�����Ϊ2��4=1��2��
��4������ͼʾ��������ķ��ӽṹ��֪�����ʵĻ�ѧʽΪ��BA3��
��5���衰 �������ԭ��������x����
�������ԭ��������x���� �������ԭ��������14x����μӷ�Ӧ��A2�������������֮��Ϊ��12��x����4����3x+14x��=3��17��
�������ԭ��������14x����μӷ�Ӧ��A2�������������֮��Ϊ��12��x����4����3x+14x��=3��17��
�ʴ�Ϊ��
��1�����Ϸ�Ӧ����2���������3��1��2����4��BA3����5��3��17��
���� �������ĸ���ȥ������ͼ�����������ʵ�ֱ��ת����������ϵ�������������ݺͽ��۵��γɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
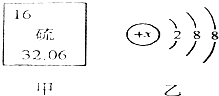
| 3 Li � 6.941 | 4 Be �� 9.012 | 5 B �� 10.81 | 6 C ̼ 12.01 | 7 N �� 14.01 | 8 O �� 16.00 | 9 F �� 19.00 | 10 Ne �� 20.18 |
| 11 Na �� 22.99 | 12 Mg þ 24.31 | 13�� �� 26.98 | 14 Si �� 28.09 | 15 P �� 30.97 | 16 S �� 32.06 | 17 Cl �� 35.45 | 18 Ar � 29.95 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȼ��ǰ�����������û�иı� | |
| B�� | ������ٵ������������ɵĶ�����̼��ˮ������ | |
| C�� | ����ȼ�պ������������֮�͵���������ٵ���������������������֮�� | |
| D�� | ȼ��ǰ�����������������������֮�͵������ɵĶ�����̼��ˮ������֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
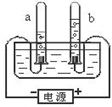 ��ͼ��ʾ���ǵ��ˮʵ��װ�ã�ͨ��һ��ʱ����������Թ��зֱ��ռ�������a������b����ش�
��ͼ��ʾ���ǵ��ˮʵ��װ�ã�ͨ��һ��ʱ����������Թ��зֱ��ռ�������a������b����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com