
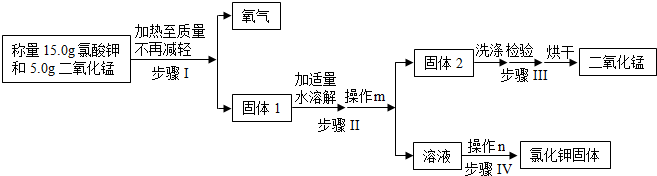
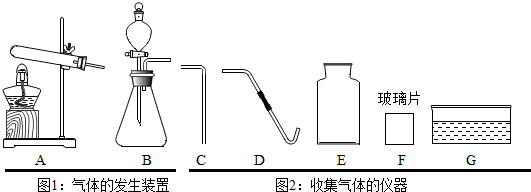
分析 (1)根据实验室用氯酸钾和二氧化锰制氧气需要加热解答;根据排水法收集的氧气较纯净解答;
(2)根据在回收提纯的过程中需要控制水的用量,是为蒸发时节约能源;
(3)步骤Ⅲ中洗涤的目的是洗去二氧化锰表面的KCl溶液解答;
(4)根据步骤Ⅳ中的操作n的名称是蒸发结晶解答;
(5)根据二氧化锰是催化剂,反应前后质量不变解答.
解答 解:
(1)实验室用氯酸钾和二氧化锰制氧气需要加热,故选A;排水法收集的氧气较纯净,所需仪器有:D、E、F、G;
(2)在回收提纯的过程中需要控制水的用量,加入适量的水一方面为了缩短蒸发时间,另一方面为蒸发时节约能源;故答案:AC;
(3)步骤Ⅲ中洗涤的目的是洗去二氧化锰表面的KCl溶液;
(4)实验室用氯酸钾和二氧化锰制氧气中,二氧化锰是催化剂,反应前后质量不变,实验结束后,理论上应回收到的二氧化锰质量为5g.
答案:
(1)A;D、E、F、G;
(2)A、C;
(3)洗去二氧化锰表面的KCl溶液;
(4)蒸发结晶;
(5)5.
点评 掌握溶解、过滤、蒸发等实验的操作技能;理解过滤法分离混合物的原理;体会过滤的原理在生活生产等社会实际中的应用.本题具有较大的综合性,在解答时需要涉及较多的基础知识,因此,需要足够的耐心和毅力.


科目:初中化学 来源: 题型:选择题
| A. | 用食醋浸泡可除去热水瓶内的水垢 | B. | 洗洁精去除油污是利用了乳化原理 | ||
| C. | 硝酸铵可用于冷敷袋中 | D. | 氢氧化钠治疗胃酸过多 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20 | B. | 32 | C. | 40 | D. | 30 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
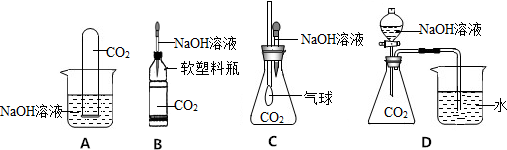
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 在装有过氧化氢溶液的试管口,放一个带火星的木条 | 木条不复燃 | 常温下过氧化氢溶液分解速率慢 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 水泥块能作过氧化氢分解的催化剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
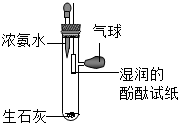 如图为某同学设计的探究分子特征的实验装置,己知:浓氨水显碱性,易挥发出氨气.氨气具有刺激性气味,酚酞遇碱溶液会变红.请按要求完成系列问题:
如图为某同学设计的探究分子特征的实验装置,己知:浓氨水显碱性,易挥发出氨气.氨气具有刺激性气味,酚酞遇碱溶液会变红.请按要求完成系列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com