
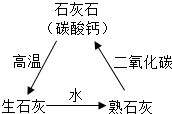
 (2010?海沧区质检)小海同学做了如下实验:ⅰ.在酒精灯上加热一片状石灰石;ⅱ.灼烧一定时间后放在石棉网上冷却;ⅲ.把冷却后的固体投入盛有适量水的小烧杯里,并用温度计测试温度的变化;ⅳ.静止后取上层清液于两支试管中,一支加入两滴酚酞试液,另一支通入二氧化碳气体;ⅴ.再向烧杯中剩余的固体上加入足量稀盐酸.实验的部分变化如图所示.回答问题:
(2010?海沧区质检)小海同学做了如下实验:ⅰ.在酒精灯上加热一片状石灰石;ⅱ.灼烧一定时间后放在石棉网上冷却;ⅲ.把冷却后的固体投入盛有适量水的小烧杯里,并用温度计测试温度的变化;ⅳ.静止后取上层清液于两支试管中,一支加入两滴酚酞试液,另一支通入二氧化碳气体;ⅴ.再向烧杯中剩余的固体上加入足量稀盐酸.实验的部分变化如图所示.回答问题:

 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:
(2010?海沧区质检)下表是某无土栽培营养液的配方(局部):已知室温20℃时,配置后的营养液密度约为1g?mL-1,现需在实验室配置1000g该营养液,下列说法不正确的是( )
|
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 大气中二氧化碳的产生 | 大气中二氧化碳的消耗 |
化石燃料的燃烧 化石燃料的燃烧 |
绿色植物的光合作用 绿色植物的光合作用 |
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源: 题型:
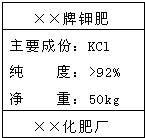 (2010?海沧区质检)“××牌”钾肥包装标签如图所示.某初三化学兴趣小组为检验该钾肥的纯度,进行了如下实验:称取3.2g该钾肥样品,加水完全溶解,加入适量AgNO3溶液至不再产生沉淀,过滤、洗涤、干燥,得到白色沉淀5.74g.
(2010?海沧区质检)“××牌”钾肥包装标签如图所示.某初三化学兴趣小组为检验该钾肥的纯度,进行了如下实验:称取3.2g该钾肥样品,加水完全溶解,加入适量AgNO3溶液至不再产生沉淀,过滤、洗涤、干燥,得到白色沉淀5.74g.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com