

| 现象 | 结论 |
| 如果装置B 澄清石灰水变浑浊 澄清石灰水变浑浊 ,装置C无现象 |
则猜想①成立 |
| 如果装置B无现象,装置C 试纸由黄色变为蓝色 试纸由黄色变为蓝色 |
则猜想②成立 |
| 如果装置B 澄清石灰水变浑浊 澄清石灰水变浑浊 ,装置C试纸由黄色变为蓝色 试纸由黄色变为蓝色 |
则猜想③成立 |
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| 现象 | 结论 |
| 如果装置B 澄清石灰水变浑浊,装置C无现象 | 则猜想①成立 |
| 如果装置B无现象,装置C 试纸由黄色变为蓝色 | 则猜想②成立 |
| 如果装置B 澄清石灰水变浑浊,装置C 试纸由黄色变为蓝色 | 则猜想③成立 |
| ||
| ||


科目:初中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
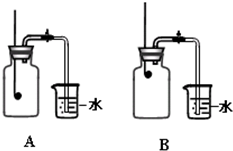 某校化学兴趣小组就空气中氧气的含量进行实验探究:
某校化学兴趣小组就空气中氧气的含量进行实验探究:| 组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 20 | 22 | 18 |
| 1 |
| 5 |
| 1 |
| 5 |
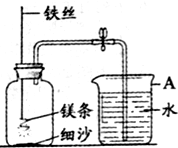 A仪器的名称是
A仪器的名称是| 点燃 |
| 点燃 |
| 点燃 |
| 点燃 |
查看答案和解析>>
科目:初中化学 来源:2011年初中毕业升学考试(广西南宁卷)化学 题型:填空题
已知浓硫酸与焦炭在加热的条件下能发生反应,生成三种氧化物。某校研究性学习小组对此进行以下一系列的探究活动。
【提出猜想】浓硫酸与焦炭在加热条件下反应,生成H2O、SO2和CO2。
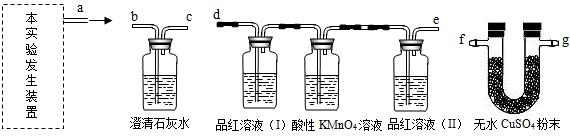
【查阅资料】经查阅资料得知:①CO2、SO2均可使澄清石灰水变浑浊;②SO2可使品红溶液的红色褪去,而CO2不能;③SO2可与酸性的KMnO4溶液反应使其褪色,而CO2不能;④无水CuSO4为白色粉末,遇水可生成蓝色胆矾。
【实验探究】用以下A—D四个装置组装成一套完整的实验装置,然后进行实验,验证猜想。
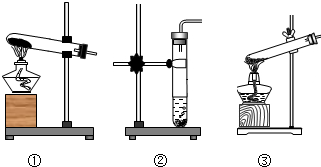
(1)本实验的发生装置应选用如下图所示三种装置中的 装置(填序号)。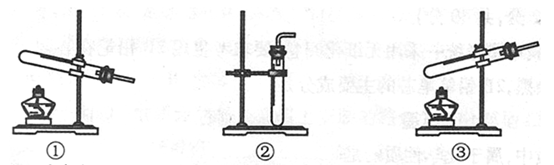
(2)为了验证三种产物,达到预期的实验目的,整套实验装置的正确组装顺序是(按导管口连接的先后顺序):发生装置导管口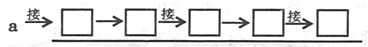
(3)实验过程中,同学们观察到装置D中的无水CuSO4变为蓝色,由此得出产物中有 的结论;同时还观察到以下实验现象:装置C中品红溶液( I)和酸性高锰酸钾溶液都褪色,品红溶液(Ⅱ)不褪色;装置B中澄清石灰水变浑浊。装置C中品红溶液( I)褪色,说明产物中有__ __,酸性KMnO4溶液的作用是____,品红溶液(Ⅱ)不褪色,说明________;装置B中发生反应的化学方程式是
(4)能确认反应产物中有CO2的实验现象是 __。
【实验结论】本实验提出的猜想____ (填“成立”或“不成立”);
浓硫酸与木炭反应的化学方程式是____ 。
【交流讨论】实验结束后,同学们针对本实验进行讨论,其中张辉同学提出了“反应产物中可能还有一氧化碳”这样的一个观点。你是否支持张辉同学的观点? _(填“支持”或“不支持”),请你说出两点理由:① ;② 。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省扬州市仪征四中九年级(上)第一次月考化学试卷(解析版) 题型:解答题
| 组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 20 | 22 | 18 |
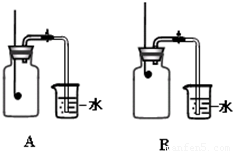
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com