
分析 (1)根据溶液稀释前后溶质的质量不变,结合题意进行分析解答.
(2)根据质量守恒定律,参加反应的各物质的质量之和等于生成的各物质的质量之和,结合题意进行分析解答.
解答 解:(1)设需要36%的浓盐酸的质量为x,根据溶液稀释前后溶质的质量不变,
则200g×18%=x×36% x=100g.
(2)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,30g氯酸钾跟6g二氧化锰混合后充分加热,冷却后称得剩余固体的质量为26.4g,由质量守恒定律,则生成氧气的质量为30g+6g-26.4g=9.6g.
故答案为:(1)100;(2)9.6.
点评 本题难度不大,掌握溶液稀释前后溶质的质量不变、质量守恒定律并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
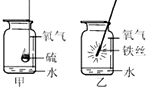
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
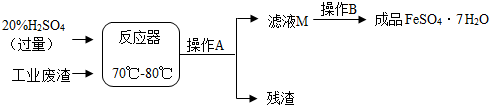
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验序号 | 过氧化氢溶液浓度、% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
| 1 | 5 | 1 | 20 | 0.1 | 4 | 16.74 |
| 2 | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| 3 | 30 | 5 | 35 | 2 | 49.21 | |
| 4 | 30 | 5 | 55 | 2 | 10.76 |
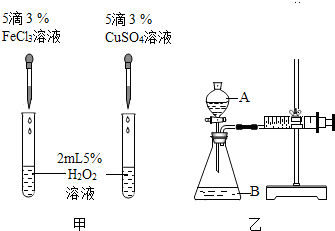
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
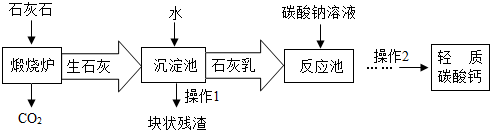
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 大理石塑像 | B. | 铝制门窗 | C. | 玻璃 | D. | 花草树木 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com