
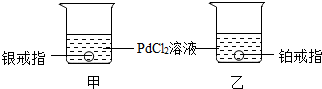
 金属钯是稀有的贵金属之一,金属钯制成的首饰不仅有迷人的光彩,而且经得住岁月磨砺.现有银(Ag)、铂(Pt)、钯(Pd)三种金属制成的戒指,某实验小组利用它们来探究三种金属的活动顺序.
金属钯是稀有的贵金属之一,金属钯制成的首饰不仅有迷人的光彩,而且经得住岁月磨砺.现有银(Ag)、铂(Pt)、钯(Pd)三种金属制成的戒指,某实验小组利用它们来探究三种金属的活动顺序.分析 (1)根据题意,将钯戒指放入稀硫酸溶液中,戒指完好无损,进行分析解答.
(2)如果将钯粉置于盐酸溶液中,边通入氧气边搅拌,钯粉溶解得到二氧化钯(PdCl2)溶液,写出反应的化学方程式即可.
(3)将银、铂戒指分别放入甲、乙两烧杯中,一段时间后取出,发现只有银戒指表面有明显变化,说明银的金属活动性比钯强,铂的金属活动性比钯弱,结合银与PdCl2溶液反应生成氯化银沉淀和钯,进行分析解答.
解答 解:(1)将钯戒指放入稀硫酸溶液中,戒指完好无损,说明钯不与稀硫酸反应,即钯排在氢的后面,可推测钯在金属活动顺序表中位于铁之后.
(2)如果将钯粉置于盐酸溶液中,边通入氧气边搅拌,钯粉溶解得到二氯化钯(PdCl2)溶液,反应的化学方程式为:2Pd+4HCl+O2═2PdCl2+2H2O.
(3)将银、铂戒指分别放入甲、乙两烧杯中,一段时间后取出,发现只有银戒指表面有明显变化,说明银的金属活动性比钯强,铂的金属活动性比钯弱,则银、铂、钯的金属活动性由强到弱顺序为银、钯、铂.
银与PdCl2溶液反应生成氯化银沉淀和钯,还会观察到有白色沉淀生成.
故答案为:(1)后;(2)2Pd+4HCl+O2═2PdCl2+2H2O;(3)有白色沉淀生成;银、钯、铂.
点评 本题难度不大,熟练掌握金属活动性顺序、化学方程式的书写方法并能灵活运用是正确解答本题的关键.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:选择题
| A. |  将久置在空气中的铝箔置入稀硫酸中 | |
| B. | 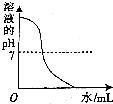 向NaOH溶液中逐滴加入水 | |
| C. | 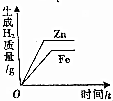 等质量的铁粉与锌粉分别与等体积等质量分数的稀硫酸(足量)反应 | |
| D. | 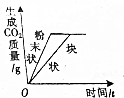 等质量的碳酸钙分别与等体积等质量分数的稀盐酸(足量)反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
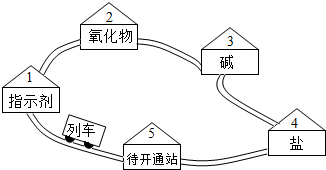 请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站.“2-5号站”各站的对应物质属于不同类别的纯净物.
请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站.“2-5号站”各站的对应物质属于不同类别的纯净物.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青蒿素属于氧化物 | B. | 1个青蒿素分子中含有11个氢分子 | ||
| C. | 青蒿素难溶于乙醚 | D. | 提取青蒿素过程中应尽量避免高温 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 胃酸过多的病人,通常需每天服用含碳酸氢钠的药物9片,能消耗胃酸中的氯化氢2.19g.某病人有胃溃疡症状,这种药物会加剧胃部疼痛.医生建议改用含氢氧化铝(其他成分不与胃酸反应)的胃舒平,药物标签如图.请计算中和相同质量的胃酸,每天需要服用胃舒平多少片?
胃酸过多的病人,通常需每天服用含碳酸氢钠的药物9片,能消耗胃酸中的氯化氢2.19g.某病人有胃溃疡症状,这种药物会加剧胃部疼痛.医生建议改用含氢氧化铝(其他成分不与胃酸反应)的胃舒平,药物标签如图.请计算中和相同质量的胃酸,每天需要服用胃舒平多少片?查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com