
| 实验步骤 | 实验现象 | 推断结果及结论 |
| (1)取一瓶气体,小心闻 其气味 | 无气味 | 瓶中的气体一定不是SO2; |
| (2)慢慢移开另一瓶的玻璃片,同时将一燃着的木条缓慢伸入瓶中 | 瓶口处未见明显现象 伸入瓶中,木条上的火焰熄灭 | 一定不是CO、CH4; 一定不是O2; |
| (3)向第三个瓶中注入少量澄清石灰水,振荡 | 石灰水变浑浊 | 你的结论:瓶中气体一定含有CO2,可能含有N2. |
分析 (1)根据二氧化硫有刺激性气味解答;
(2)根据甲烷、一氧化碳有可燃性,氧气有助燃性回答.
(3)根据二氧化碳能和氢氧化钙反应从而使澄清的石灰水变浑的性质回答.
解答 解:
(1)取一瓶气体,小心闻其气味,无气味,瓶中的气体一定不是SO2;
(2)慢慢移开另一瓶的玻璃片,同时将一燃着的木条缓慢伸入瓶中,瓶口处未见火焰,说明一定不是可燃性气体CO、CH4;木条熄灭,说明气体不支持燃烧,一定不是氧气;
(3)向第三个瓶中注入少量澄清石灰水,振荡,澄清的石灰水变浑,则一定是二氧化碳CO2,氮气不支持燃烧,可能含有氮气.
答案:
| 验步骤 | 实验现象 | 推断结果及结论 |
| (1)取一瓶气体,小心闻 其气味 | 无气味 | 瓶中的气体一定不是 SO2; |
| (2)慢慢移开另一瓶的玻璃片,同时将一燃着的木条缓慢伸入瓶中 | 瓶口处未见明显现象 伸入瓶中,木条上的火焰熄灭 | 一定不是 CO、CH4; 一定不是 O2; |
| (3)向第三个瓶中注入少量澄清石灰水,振荡 | 石灰水变浑浊 | 你的结论:瓶中气体一定含有CO2,可能含有N2. |
点评 气体的检验是化学实验部分的重要考点之一,是中考中出现频度较高的试题,要引起高度重视.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ①②③ | C. | ③④⑤ | D. | ①③ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH、BaCl2、Na2SO4 | B. | Na2CO3、NaCl、Na2SO4 | ||
| C. | CuSO4、NaCl、NaNO3 | D. | Na2SO4、HCl、NaNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 单质是由同种元素组成的,所以由同种元素组成的物质一定是单质 | |
| B. | 通常酸的溶液pH<7,碱的溶液pH>7,但是盐的溶液pH不一定等于7 | |
| C. | 碳酸盐与稀盐酸反应产生气体,所以与稀盐酸反应产生气体的物质一定是碳酸盐 | |
| D. | 二氧化碳的大量排放会增强地球的温室效应,所以二氧化碳是空气污染物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 洗脸、涮牙时不间断地放水 | B. | 洗澡擦肥皂时不关喷头,任水流 | ||
| C. | 任由水龙头漏水而不及时修理 | D. | 洗菜、淘米的水用来浇花 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
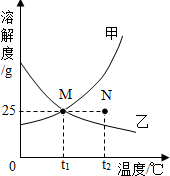
| A. | t2时,将甲乙两种物质的饱和溶液降低至t1,仍为饱和溶液 | |
| B. | t1时,甲乙饱和溶液的溶质质量分数为20% | |
| C. | 甲物质中混有少量乙,可采用蒸发溶剂方法提纯甲 | |
| D. | t2时,N点表示乙物质的不饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
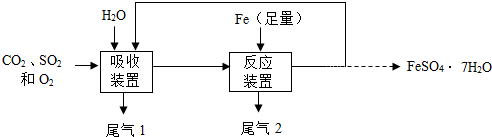
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com