
除去食盐水中的CaCl2、和Na2SO4和MgCl2杂质的操作有:①加过量的BaCl2溶液;②过滤;③加过量Na2CO3溶液;④蒸发结晶;⑤加适量盐酸;⑥加过量Ca(OH)2溶液;。下列操作顺序正确的是(提示BaSO4、BaCO3难溶于水)
A. ①③⑥②⑤④ B. ⑥①⑤③②④ C. ⑥①③⑤④② D. ①⑥③②⑤④
D 【解析】硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,加过量Ca(OH)2溶液可以将镁离子转化为沉淀,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为:①⑥③②⑤④。故选D。科目:初中化学 来源:2018年福建省永春县化学质检试卷 题型:单选题
下列实验方法不能达到实验目的的是
选项 | 实验目的 | 实验方法 |
A | 证明NaOH溶液中含有Na2CO3 | 滴加无色酚酞试剂 |
B | 除去 CO2中少量CO | 将混合气体通过足量灼热的CuO |
C | 鉴别石灰水和NaOH溶液 | 加入适量的碳酸钠溶液 |
D | 比较 Fe、Cu、Ag的金属活动性 | 将 Fe和 Ag分别放入 CuSO4溶液中 |
A. A B. B C. C D. D
A 【解析】A、氢氧化钠溶液和碳酸钠溶液均呈碱性,均能使无色的酚酞变成红色,错误;B、一氧化碳具有还原性,可还原氧化铜生成二氧化碳,正确;C、澄清石灰水的主要成分是氢氧化钙,氢氧化钙能与碳酸钠反应生成碳酸钙沉淀,氢氧化钠不能与碳酸钠反应,正确;D、根据金属活动性顺序的应用:位于前面的金属能把位于后面的金属从化合物的溶液中置换出来,比较 Fe、Cu、Ag的金属活动性,可将 Fe和 Ag分别放入...查看答案和解析>>
科目:初中化学 来源:四川省资阳市毕业班适应性检测化学试卷 题型:简答题
从“丝绸之路”到“一带一路”的倡议,促进了东西方经济、文化的交流。
(1)“丝绸之路”把中国的丝绸、茶叶等传入西方,将西方的宝石等带入中国。丝绸裁剪缝制的过程是____(选填“物理”或“化学”)变化;新鲜茶叶中含维生素C,其化学式是C6H8O6,维生素C中各元素的原子个数最简整数之比为__________;宝石的成分复杂,其中所含的Al2O3根据物质分类属于______。(多选项,选填序号)
①化合物 ②单质 ③无机化合物 ④有机化合物 ⑤纯净物 ⑥氧化物
(2)能源合作是“一带一路”的重要内容,中缅油气管道将石油和天然气输入中国。石油是由多种化合物组成的 ______(选填“混合物”或“纯净物”);天然气的主要成分是甲烷(化学式是CH4)请写出甲烷燃烧的化学方程式 _________________________。
物理 3:4:3 ①③⑤⑥ 混合物 CH4+2O2 CO2+2H2O 【解析】本题考查了化学变化和物理变化的判别,化学式的含义,物质的分类,化学方程式的书写等。 (1)丝绸裁剪的过程中没有新物质生成,属于物理变化;根据维生素C的化学式可知,维生素C中各元素的原子个数最简整数之比=3:4:3;氧化铝(Al2O3)是由一种物质组成,属于纯净物,是由不同种元素组成纯净物属于化合物,是由两种元...查看答案和解析>>
科目:初中化学 来源:河南省邓州市2018届九年级中考第二次模拟考试化学试卷 题型:填空题
现有6.4g未知物和氧气充分反应,经测定生成4.4g二氧化碳,2.8g一氧化碳和7.2g水。则参加反应氧气的质量是________,生成的二氧化碳和水的分子个数之比为_________。
8g 1:4 【解析】氧气质量为4.4g+2.8g+7.2g-6.4g=8g;生成的二氧化碳和水的分子个数之比= :=1:4。查看答案和解析>>
科目:初中化学 来源:河南省邓州市2018届九年级中考第二次模拟考试化学试卷 题型:单选题
除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是
物 质 | 杂质(少量) | 加入试剂及用量 | 除杂操作方法 | |
A | KCl溶液 | CaCl2 | 适量的Na2CO3溶液 | 过滤、除去滤渣 |
B | NaCl | Na2CO3 | 过量的盐酸 | 加热蒸发 |
C | Cu(NO3)2 | AgNO3 | 足量铜粉 | 过滤将滤渣烘干 |
D | N2 | O2 | 足量的碳粉 | 加热 |
A. A B. B C. C D. D
B 【解析】A、Na2C03溶液和氯化钙反应会生成氯化钠,带入新的杂质,错误;B、碳酸钠和盐酸反应生成氯化钠、二氧化碳、水,能除杂,过量的盐酸通过蒸发结晶除掉,正确;C、铜和硝酸银反应生成硝酸铜和银,过滤后,将滤液蒸发结晶得硝酸铜固体,错误;D、碳和氧气反应生成二氧化碳,引入新的杂质,错误。故选B。查看答案和解析>>
科目:初中化学 来源:河南省邓州市2018届九年级中考第二次模拟考试化学试卷 题型:单选题
我们生活在不断变化的物质世界里。下列变化一定属于化学变化的是
A. 用干冰进行人工降雨 B. 铁制品在潮湿空气中生锈
C. 用空气作原料制取氧气 D. 固体物质加热后全部变成气体
B 【解析】A、用干冰进行人工降雨是利用干冰升华吸热,使周围温度降低,水蒸气冷凝成水滴,属于物理变化,故A错;B、铁制品在潮湿空气中生锈,生成了主要成分是氧化铁的新物质,属于化学变化,故B正确;C、用空气作原料制取氧气是利用分离液态空气法,属于物理变化,故C错;D、固体物质加热后全部变成气体,可能是化学变化,也可能是物理变化,故D错。故选B。查看答案和解析>>
科目:初中化学 来源:河南省周口市2018届九年级下学期期末学业考试化学试卷 题型:填空题
如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答:
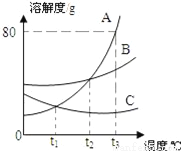
(1)t3℃时,50g水中加入50gA物质形成溶液的质量为____ 。
(2)要将t3℃时A B C三种物质的饱和溶液降温到t1℃时三种溶液中溶质的质量分数由大到小的顺序是_____________。
90g B > A > C 【解析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。(1)通过分析溶解度曲线可知,t3℃时,A物质的溶解度是80g,所以50g水中加50g物质形成溶液...查看答案和解析>>
科目:初中化学 来源:江苏省泰兴市2018届九年级中考二模化学试卷 题型:科学探究题
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后锥形瓶中残留废液进行探究。

(提出问题)废液中所含溶质是什么物质?
(猜想与假设)
猜想1:废液中的溶质可能是NaCl、Na2CO3和HCl。 猜想2:废液中的溶质只有NaCl。
猜想3:废液中的溶质是NaCl和HCl。 猜想4:废液中的溶质是______。
(讨论与交流)
小明认为猜想1无需验证就知道是错误的。他的理由是______。
(实验与结论)
(1)为验证猜想2,小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是小强认为猜想2正确。小强的实验______(填“能”或“不能”)验证猜想2的正确性,原因是______。
(2)小丽为验证猜想3,选锌粒做试剂。若猜想3是正确的,验证时反应的化学方程式为______。
(3)若验证猜想4是否正确,下列试剂中可选用的有______(填序号)。
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
(拓展与应用)
(4)若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行______操作即可从废液中得到NaCl固体。此方法的缺点是______。
Na2CO3和NaCl 在溶液中Na2CO3和HCl不能共存 不能 溶液中若有HCl,遇AgNO3溶液也能产生不溶于稀HNO3的白色沉淀 Zn+2HCl=ZnCl2+H2↑ ②③ 蒸发 挥发出的HCl气体会污染空气 【解析】本题通过实验探究物质的组成成分考查了酸、盐的化学性质。通过现象判断物质是否存在,要排除同类离子的干扰。 猜想与假设:盐酸与碳酸钠反应生成氯化钠、水、二氧化碳。恰好完...查看答案和解析>>
科目:初中化学 来源:宁夏银川市2018届九年级下学期第二次模拟考试化学试卷 题型:简答题
王明觉得你很聪明,是他的良师益友,学完“酸的化学性质”后,邀请你与他讨论“食醋在厨房中的妙用”:
(1)复习酸的化学性质
①酸与指示剂作用 | 酸溶液能使紫色石蕊溶液变红色 | 酸溶液不能使无色酚酞溶液变色 |
②酸与活泼金属作用 | Fe+2HCl=FeCl2+H2↑ | Fe+H2SO4=FeSO4+H2↑ |
③酸与某些金属氧化物作用 | Fe2O3+HCl=FeCl2+H2O | …… |
④酸与碱作用 | ||
...... |
由于王明的课堂笔记没做好,“③酸与某些金属氧化物作用”后面的化学方程式书写错误,请帮他写出正确的化学方程式:_______________________________。
(2)讨论交流
(Ⅰ)王明自豪地说,目前世界卫生组织正在推广使用中国铁锅,使用铁锅炒菜时,放点食醋时,可以补充人体需要的微量元素______元素,该反应的原理是利用了酸的化学性质_________(填序号“①”、“②”或“③”)。铁与的稀盐酸反应后,溶液中的溶质可能含有HCl,下列物质能证明是___________
A.CuO B.AgNO3溶液 C.Cu D.NaOH溶液
(Ⅱ)你告诉王明,他总结的酸的化学性质④酸与碱作用,这类化学反应的基本反应类型是____________ 。
(3)反思
盐酸、硫酸、食醋具有相似化学性质的原因是因为它们的水溶液中都含有_______。(填符号)
Fe2O3+6HCl=2FeCl3+3H2O 铁 ② A 复分解反应 H+ 【解析】本题主要考查酸的化学性质及具有相似化学性质的原因。 (1)复习酸的化学性质:氧化铁与盐酸发生复分解反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl=2FeCl3+3H2O; (2)(Ⅰ) ①推广使用中国铁锅,使用铁锅炒菜时能补充人体需要的微量元素铁元素;该反应的原理是利用了酸与活泼金属...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com