
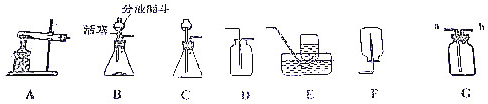
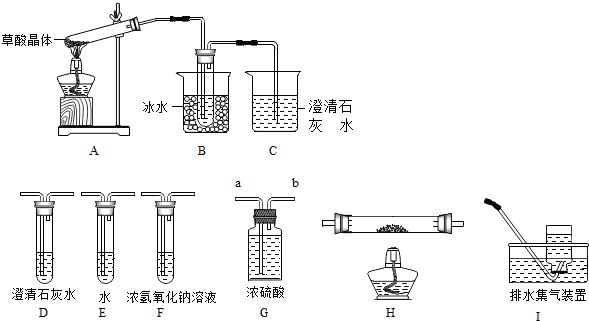
 于排水法收集氧气,可在G中装满水后,将氧气从b口(“a”或“b”)进入.
于排水法收集氧气,可在G中装满水后,将氧气从b口(“a”或“b”)进入.分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,易溶于水,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(3)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,分液漏斗可以控制液体的滴加速度,氧气密度比水小进行分析;
(4)根据微型装置中各种仪器的作用进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,有试管、酒精灯等;
(2)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以发生装置应选B或C,二氧化碳密度比空气大,易溶于水,所以收集装置应选D,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,分液漏斗可以控制液体的滴加速度,所以发生装置选用B而不选C,其原因是:便于可知反应的速率,氧气密度比水小,所以可在G中装满水后,将氧气从b口进入;
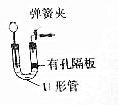
(4)右图微型装置可用于制取H2,其中U形管相当于上图C中锥形瓶,使用该装置的优点是:①节约药品;②可以控制反应的发生和停止.
故答案为:(1)试管、酒精灯等;
(2)B或C,D,CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,便于可知反应的速率,b;
(4)锥形瓶,可以控制反应的发生和停止.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


科目:初中化学 来源: 题型:解答题
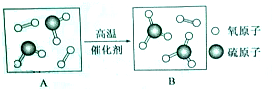
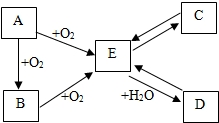 A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体.其转化关系如图所示:
A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体.其转化关系如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
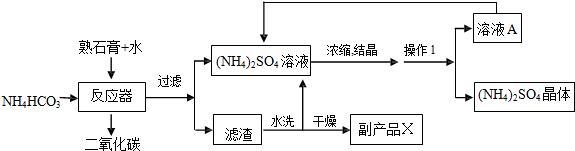
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青蒿素是有机高分子化合物 | B. | 青蒿素的相对分子质量为282 | ||
| C. | 青蒿素中含量最多元素是氢元素 | D. | 青蒿素在高温下性质稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com