
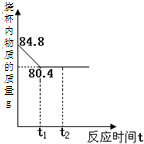
 工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠,现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应,反应过程中烧杯内物质的质量随时间的变化关系如图所示.求:样品中碳酸钠的质量分数.
工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠,现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应,反应过程中烧杯内物质的质量随时间的变化关系如图所示.求:样品中碳酸钠的质量分数.| 106×4.4g |
| 44 |
| 10.6g |
| 11.8g |


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源: 题型:
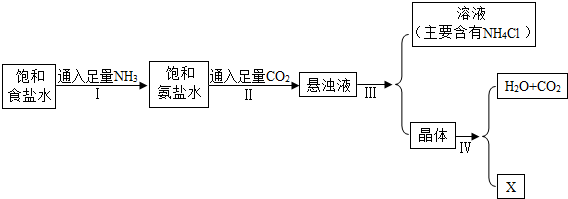
| 操作步骤 | 现象 | 结论 |
| (1)取该晶体加熟石灰研磨 | 无氨味 | 猜想 3和5 3和5 不成立 |
| (2)另取该晶体加入盐酸 | 有气泡产生 有气泡产生 |
猜想1不成立 |
| (3)另取少量该晶体加水溶解,再滴入氯化钙溶液 | 无白色沉淀 | 猜想4不成立 |
(4)另取该固体放入如图试管中加热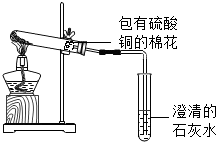 |
包有硫酸铜的棉花变 蓝色 蓝色 色,石灰水变浑浊 浑浊 |
综合(1)、(2)、(3)的结论得出猜想2成立 |
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com