
【题目】根据下列装置,结合所学化学知识回答下列问题:

(1)写出图中标号仪器的名称:①___________;②___________;
(2)实验室用双氧水和二氧化锰制取氧气时,如需随时控制反应速率并节约药品,发生装置最好选用___,收集装置选用___,能用此收集方法的原因是______________,写出该反应的文字表达式_____________,二氧化锰是该反应的__________。
(3)实验室用高锰酸钾制取氧气时,发生装置应选用__________(填字母);其反应的文字表达式或符号表达式是_____________,二氧化锰是该反应的_____。
(4)氨气极易溶于水,且密度比空气小,实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,应用_________装置,收集氨气最好用________装置。
(5)为了测量生成氧气的体积可用如图装置,氧气从__________端进入(填序号),量筒的作用是________。装置内的空气对测量结果_________(填“有影响”或“无影响”)

【答案】长颈漏斗 试管 B E(或G) 氧气密度比空气大(或氧气不易溶于水) 过氧化氢 ![]() 水+氧气 催化剂 C 高锰酸钾
水+氧气 催化剂 C 高锰酸钾![]() 锰酸钾 + 二氧化锰 + 氧气 生成物 C F d 测量排出水的体积,从而得出收集的氧气体积 无影响
锰酸钾 + 二氧化锰 + 氧气 生成物 C F d 测量排出水的体积,从而得出收集的氧气体积 无影响
【解析】
(1)长颈漏斗方便加液体药品,试管是常用的反应容器,故答案为:①长颈漏斗,②试管
(2)如果用双氧水和二氧化锰制氧气就不需要加热,其中二氧化锰起催化作用;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气;故答案为:B;E(或G);氧气密度比空气大(或氧气不易溶于水);过氧化氢![]() 水+氧气;催化剂;
水+氧气;催化剂;
(3)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,其中二氧化锰是生成物,故答案为:C;高锰酸钾![]() 锰酸钾+二氧化锰﹢氧气;生成物。
锰酸钾+二氧化锰﹢氧气;生成物。
(4)实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,发生装置为固-固加热型;氨气极易溶于水,且密度比空气小,因此只能用向下排空气法收集;故答案为:C;F。
(5)为了测量生成氧气的体积可用如图2装置,氧气从短管进入,因为氧气的密度比水小;量筒的作用是:测量排出水的体积,从而得出收集的氧气体积;装置内的空气对测量结果无影响,因为进入氧气后,压强增大,才把水排出来;故答案为:d;测量排出水的体积,从而得出收集的氧气体积;无影响。


科目:初中化学 来源: 题型:
【题目】某品牌牙膏中的摩擦剂是经过一系列加工而制得的极细小的碳酸钙粉末,它的生产过程如下:

(1)请写出A物质的名称___________(或化学式)
(2)请从①②③三个反应中选择一个,写出反应的化学方程式_____________________。
(3)二氧化碳有许多用途,请举出其中一例__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E五种物质都有人体内含量最高的一种金属元素,其中A是单质,B、C含有两种元素,D、E含有三种元素,反应⑤是放热反应,它们之间的转化关系如图所示,下列推理不正确的是( )

A. E是碳酸钙
B. 反应④一定是中和反应
C. 反应③可以由多个化学反应实现
D. 反应②是吸热反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在如图有关物质转化关系中,各物质均是初中化学常见的物质,其中A为红色金属单质,B能参与植物的光合作用![]() 、D为黑色粉末,F为可用于改良酸性土壤的碱,G为难溶性物质,H为难溶性蓝色物质
、D为黑色粉末,F为可用于改良酸性土壤的碱,G为难溶性物质,H为难溶性蓝色物质![]() 图中部分生成物已省略
图中部分生成物已省略![]() .
.
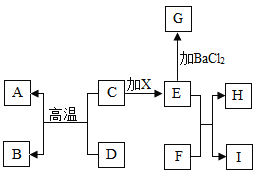
![]() 用化学式表示:D______G______
用化学式表示:D______G______
![]() 写出E与F反应的化学方程式______
写出E与F反应的化学方程式______
![]() 光合作用生成的淀粉在人体内变成葡萄糖
光合作用生成的淀粉在人体内变成葡萄糖![]() ,葡萄糖在酶的催化作用下发生缓慢氧化,同时放出热量,写出葡萄糖发生缓慢氧化反应的化学方程式______.
,葡萄糖在酶的催化作用下发生缓慢氧化,同时放出热量,写出葡萄糖发生缓慢氧化反应的化学方程式______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们的生活离不开空气。
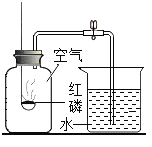
初中阶段,我们用如图所示的装置和药品研究空气的组成。写出发生反应的文字表达式:___________;实验过程中,燃着的红磷熄灭后,当冷却至室温时,水能进入集气瓶中,其原因为___________。若实验中测得氧气的体积分数低于理论值,则造成此误差的可能原因有哪些?__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生产、生活中常需配制溶液.

(1)配制一瓶如图所示溶液需氯化钠_____g.
(2)配制一定质量分数的氯化钠溶液时,下列哪些操作会导致溶液的质量分数偏小______?请说明偏小的原因________________________。
①用量筒量取水时仰视读数;
②往烧杯中加水时有水溅出;
③称量含不溶性杂质的氯化钠来配制溶液;
④将配制好的溶液往试剂瓶中转移时有少量溅出.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
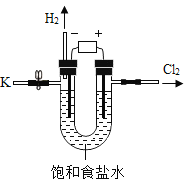
老师提示:
I.电解饱和食盐水的化学方程式:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对本实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
实验步骤 | 实验现象 | 实验结论 |
____________________ | ________________ | 待测液中含有氢氧化钠. |
探究活动二:测定待测液中氢氧化钠的质量分数
(实验1)用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
(2)写出待测液中的氢氧化钠与稀盐酸反应的化学方程式:________________________.
(3)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据计算所称取待测液中氢氧化钠的质量时,应选用稀盐酸的体积为_______________mL.
(实验2)用沉淀法测定
资料摘要:氢氧化钠与氯化镁在溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
取待测液称重 ②加入足量氯化镁溶液 ③过滤出沉淀物 ④洗涤沉淀 ⑤干燥称重
乙组同学按如图所示的实验步骤进行实验:
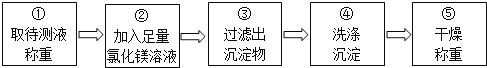
(4)步骤②加入的氯化镁溶液必需足量,其目的是____________________.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:___________________________(写出实验步骤、现象和结论).
(5)步骤③过滤出的沉淀物是____________.
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将 ________(选填“偏大”、“偏小”或“没影响”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁是四个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:

(1)依据丙实验回答:
①小明实验前将铁丝绕成螺旋状的目的是________________________________。
②铁丝在氧气中燃烧的文字表达式_____________________________。
(2)甲、丙两实验集气瓶中均放少量水,甲中加入少量水的目的是_________________。
通过甲、丙两个实验,结合课堂学习,你认为在“集气瓶中进行燃烧的实验”应该注意的问题是(说明一点即可)________________________。
(3)小明做完上述实验后,在乙中加入澄清石灰水,目的为验证_____________。
(4)小明用图丁中的方法测定空气中氧气的含量,结果偏低(装置不漏气),其主要原因是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】沙东化工厂的废水中含有HCl和FeCl3再无其他杂志.小明同学采集了该废水样品80.7g,向其中滴加20%的NaOH溶液至溶液沉淀完成时消耗该NaOH溶液80g.待溶液冷至常温,测得其pH=7.将生成的沉淀滤出,经水洗,干燥后称重为10.7g.
(1)上述废水样品反应后所得的溶液中,溶质是(写化学式,下同)___,溶剂是___,阴、阳离子所带的负电荷总数和正电荷总数之比为____.
(2)已知上述反应后的溶液在常温下为不饱和溶液,请计算其中溶质的质量分数____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com