
| 实验内容 | 实验设计 | |
| A | 验证某溶液为稀盐酸 | 先测溶液的pH<7,再加入锌粒 |
| B | 提纯久置变质的NaOH溶液 | 加入足量CaCl2溶液,充分反应后,过滤 |
| C | 除去H2中混有的少量水蒸气、HCl | 先通过浓H2SO4,再通过NaOH溶液 |
| D | 分离CO2、CO混合物 | 先用NaOH溶液吸收掉CO2分离出CO,再向该NaOH溶液加足量稀盐酸“释放”出CO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据酸能与活泼金属反应,pH<7,进行分析判断.
B、变质的NaOH溶液中含有生成的碳酸钠,据此进行分析判断.
C、除去H2中混有的少量水蒸气、HCl,应先除去氯化氢气体,再除去水蒸气,据此进行分析判断.
D、根据二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,一氧化碳不与氢氧化钠溶液反应,碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳,进行分析判断.
解答 解:A、酸能与活泼金属反应,先测溶液的pH<7,再加入锌粒,验证某溶液不一定为稀盐酸,也可能是硫酸等酸,应选用硝酸银溶液检验是否含有氯离子,故选项实验设计不能达到目的.
B、变质的NaOH溶液中含有生成的碳酸钠,加入足量CaCl2溶液,碳酸钠与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,引入了新的杂质氯化钠,故选项实验设计不能达到目的.
C、除去H2中混有的少量水蒸气、HCl,应先除去氯化氢气体,再除去水蒸气,否则再通过NaOH溶液时,又引入了水蒸气,故选项实验设计不能达到目的.
D、分离CO2、CO混合物,先用NaOH溶液吸收掉CO2分离出CO,再向该NaOH溶液加足量稀盐酸,碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳,“释放”出CO2,故选项实验设计能达到目的.
故选:D.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.


科目:初中化学 来源: 题型:多选题
| A. |  金属铁具有导热性,用于制作铁桶 | |
| B. |  活性炭具有吸附性,用作防毒面具 | |
| C. |  氧气具有可燃性,用作火箭燃料 | |
| D. |  洗涤剂具有乳化功能,用于除去油污 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气和液氢都可做燃料--相同物质的分子,其化学性质相同 | |
| B. | 金刚石和石墨物理性质存在差异,是因为它们的原子排列方式不同 | |
| C. | 水烧开后易把壶盖冲起--温度升高,水分子间隔变大 | |
| D. | 春天柳絮四处飘飞--分子在不断的运动 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
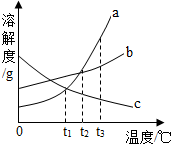 如图是a、b、c三种物质的溶解度曲线.
如图是a、b、c三种物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com