
| �¶ȣ��棩 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| KNO3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 |
| NaCl | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 |
 ��100%=26.5%�����26.5%��
��100%=26.5%�����26.5%��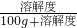 ��100%���������ʵ��ܽ�ȵı仯�Լ��ܽ�ȵó���صĽ��ۣ�
��100%���������ʵ��ܽ�ȵı仯�Լ��ܽ�ȵó���صĽ��ۣ�

 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� ���� |
OH- | NO3- | Cl- |
| Na+ | �� | �� | �� |
| K+ | �� | �� | �� |
| Ag+ | - | �� | �� |
| H+ | - | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
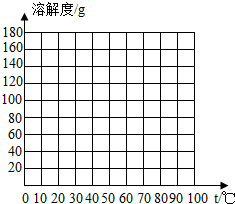
�¶ȣ��棩 �ܽ�ȣ�g�� |
0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�±��Dz������ʵ��ܽ��Ա���20�棩�����ñ����ṩ����Ϣ�ش��������⣨��-����ʾ�������ʲ����ڻ���ˮ�ͷֽ��ˣ���
| ���� ���� | OH- | NO3- | Cl- |
| Na+ | �� | �� | �� |
| K+ | �� | �� | �� |
| Ag+ | - | �� | �� |
| H+ | - | �� | �� |
��1��NaOH��KNO3�������ʻ�Ϻ��ܷ�����Ӧ��________Ϊʲô��________��
��2��д��һ���кͷ�Ӧ�Ļ�ѧ����ʽ��________��
��3��д��һ���г������ɵĸ��ֽⷴӦ�Ļ�ѧ����ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
| ���� ���� |
OH- | NO3- | Cl- |
| Na+ | �� | �� | �� |
| K+ | �� | �� | �� |
| Ag+ | - | �� | �� |
| H+ | - | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��2����������Ӣ��ѧУ�п���ѧģ���Ծ��������������棩 ���ͣ������
| ���� ���� | OH- | NO3- | Cl- |
| Na+ | �� | �� | �� |
| K+ | �� | �� | �� |
| Ag+ | - | �� | �� |
| H+ | - | �� | �� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com