
分析 其中辣味属于味道是物理性质,氢氧化锂(化学式LiOH)的化学性质与NaOH相似,可知它也属于碱类,具有碱的通性:①水溶液中能电离出氢氧根离子②能与酸反应③能与二氧化碳反应④能与某些盐反应.又CO2+2NaOH═Na2CO3+H2O可以推断出LiOH与CO2的反应方程式.
解答 解:(1)物质没有发生化学变化就表现出来到性质.通常物质的物理性质就是指色味态密熔沸以及溶解度.
(2)根据氢氧化锂(化学式LiOH)的化学性质与NaOH相似,NaOH属于碱,故它也属于碱;
(3)结合LiOH和NaOH都呈碱性,所以水溶液中都能使紫色石蕊溶液变红色;
(4)根据氢氧化钠和二氧化碳反应的化学方程式可推断,CO2+2LiOH═Li2CO3+H2O
故正确答案:(1)物理;(2)碱;(3)红色;(4)CO2+2LiOH═Li2CO3+H2O.
点评 本题以航天用的金属锂为信息,引入氢氧化锂进而来,探究这种物质的性质和用途;看似比较陌生的一种物质实质上只要掌握氢氧化钠的特性,将所学知识进行迁移即可,灵活应用.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 20℃时,100g水中最多能溶解氯化钠36g | |
| B. | 20℃时,氯化钠饱和溶液中水与氯化钠的质量比为100:36 | |
| C. | 20℃时,100g氯化钠饱和溶液中含氯化钠36g | |
| D. | 20℃时,将36g氯化钠溶解于100g水中,所得溶液为该温度下氯化钠的饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水分子是由氢离子和氢氧根离子构成的 | |
| B. | 电解水的实验中,得到的氢气与氧气体积比为2:1 | |
| C. | 过滤、吸附、蒸馏是常用的净水方法 | |
| D. | 地球上的水储备是丰富的,全可供利用的淡水资源是有限的 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
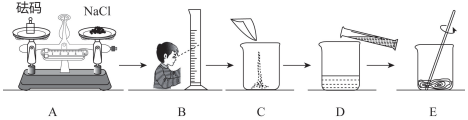
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
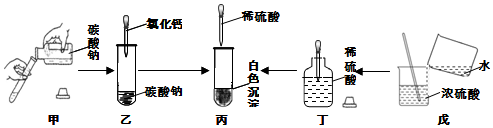
| A. | 甲中试剂瓶标签正对手心,是为了防止手被腐蚀 | |
| B. | 乙中将滴管伸入试管内,是为了防止试剂滴落到试管外 | |
| C. | 丁中试剂瓶盖倒放在桌面上,主要是为了避免瓶中试剂受污染 | |
| D. | 戊中将水缓缓倒入浓硫酸并搅拌,是为了防止局部过热引起酸液飞溅 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食用瘦肉等含铁食物预防缺铁性贫血 | |
| B. | 医疗上用氯化钠配制生理盐水 | |
| C. | 用二氧化碳灭火器扑灭图书、档案等物品的失火 | |
| D. | 用聚氯乙烯塑料制成食品保鲜膜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com